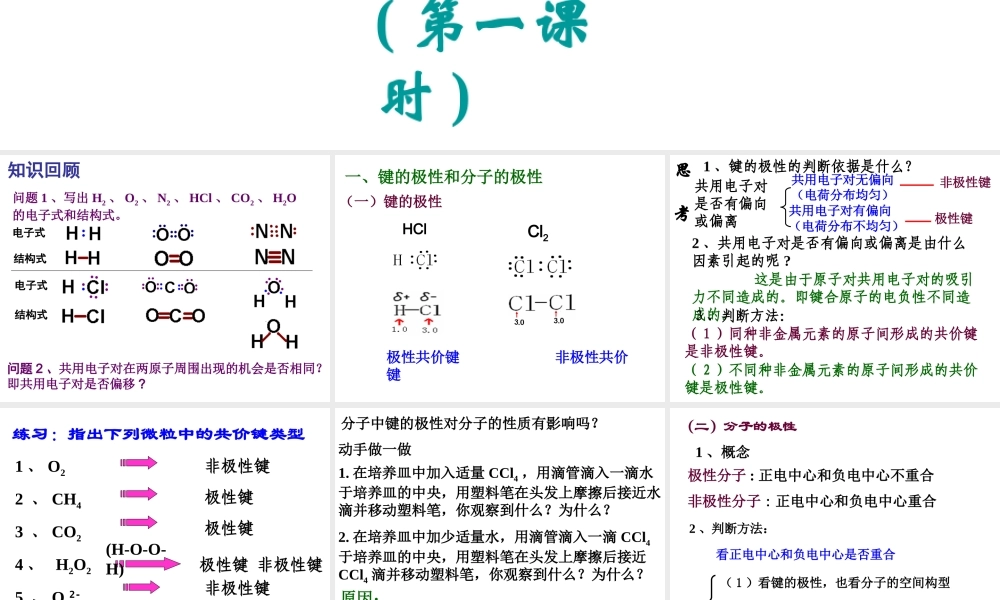
第二章分子结构与性质(第一课时)第三节分子的性质知识回顾问题1、写出H2、O2、N2、HCl、CO2、H2O的电子式和结构式。问题2、共用电子对在两原子周围出现的机会是否相同?即共用电子对是否偏移?电子式结构式电子式结构式极性共价键非极性共价键一、键的极性和分子的极性(一)键的极性HClCl22、共用电子对是否有偏向或偏离是由什么因素引起的呢?这是由于原子对共用电子对的吸引力不同造成的。即键合原子的电负性不同造成的。1、键的极性的判断依据是什么?共用电子对是否有偏向或偏离思考共用电子对有偏向(电荷分布不均匀)共用电子对无偏向(电荷分布均匀)非极性键极性键3、判断方法:(1)同种非金属元素的原子间形成的共价键是非极性键。(2)不同种非金属元素的原子间形成的共价键是极性键。练习:指出下列微粒中的共价键类型1、O22、CH43、CO24、H2O25、O22-6、OH-非极性键极性键极性键(H-O-O-H)极性键非极性键非极性键极性键1.在培养皿中加入适量CCl4,用滴管滴入一滴水于培养皿的中央,用塑料笔在头发上摩擦后接近水滴并移动塑料笔,你观察到什么?为什么?2.在培养皿中加少适量水,用滴管滴入一滴CCl4于培养皿的中央,用塑料笔在头发上摩擦后接近CCl4滴并移动塑料笔,你观察到什么?为什么?原因:说明H2O分子与CCl4分子不同,H2O分子受静电作用,CCl4分子不受静电动手做一做分子中键的极性对分子的性质有影响吗?极性分子:正电中心和负电中心不重合非极性分子:正电中心和负电中心重合看正电中心和负电中心是否重合(2)化学键的极性的向量和是否等于零(1)看键的极性,也看分子的空间构型2、判断方法:1、概念(二)分子的极性第一类:全部由非极性键组成的分子是非极性分子。如:P4、C60、S8C70、B12第二类:对于ABn型分子极性判别方法由极性键组成的双原子分子一定是极性分子。1.双原子分子双原子分子的极性取决于成键原子之间的共价键是否有极性,且分子的极性与键的极性一致。由非极性键组成的双原子分子一定是非极性分子。多原子分子呢?C=O键是极性键,但从分子总体而言CO2是直线型分子,两个C=O键是对称排列的,两键的极性互相抵消(F合=0),∴整个分子电荷分布均匀,没有极性,是非极性分子180ºF1F2F合=0OOCCO2HOH105ºF1F2F合≠0O-H键是极性键,共用电子对偏O原子,由于分子是V形构型,两个O-H键的极性不能抵消(F合≠0),∴整个分子电荷分布不均匀,是极性分子H2OHHHNBF3NH3120º107º三角锥型,不对称,键的极性不能抵消,...