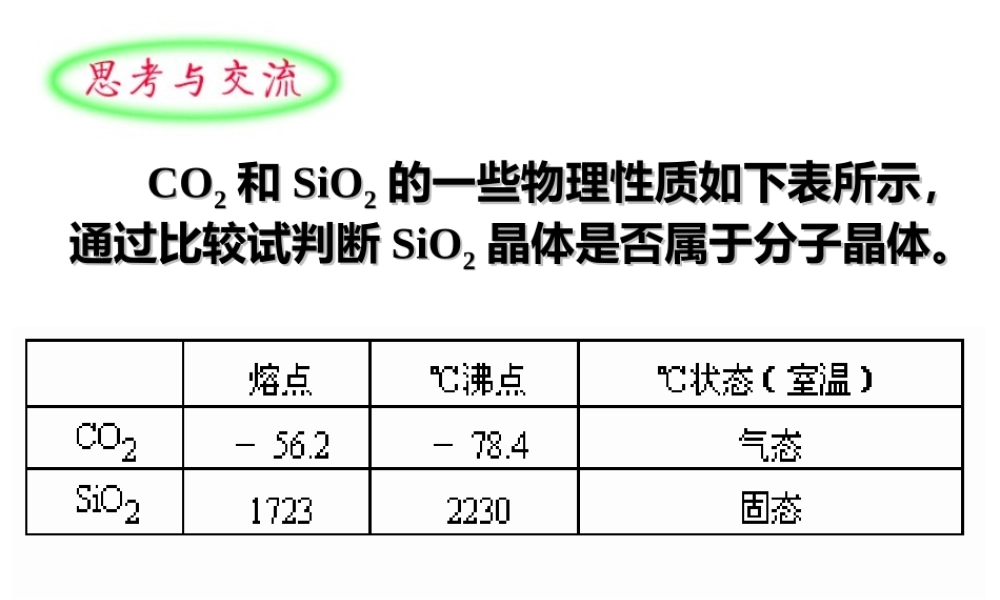
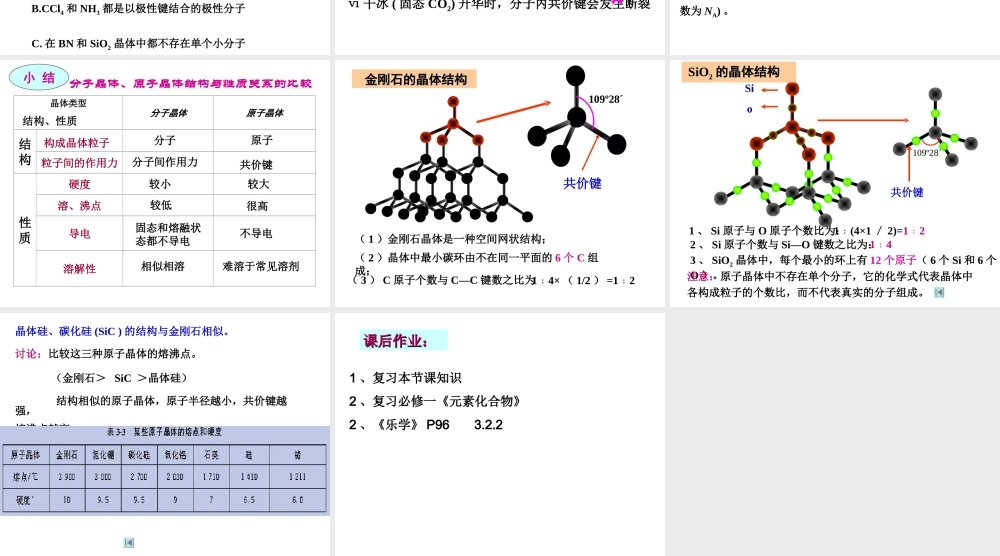
COCO22和和SiOSiO22的一些物理性质如下表所示,的一些物理性质如下表所示,通过比较试判断通过比较试判断SiOSiO22晶体是否属于分子晶体。晶体是否属于分子晶体。二、原子晶体二、原子晶体相邻原子间以共价键相结合而形成空间网状结构的晶体。原子。共价键1、构成微粒:2、晶体中微粒间的作用力:3、原子晶体物理性质的共性:熔点和沸点高,硬度大,一般不导电,难溶于一些常见的溶剂。原子晶体的熔沸点的高低的比较:原子晶体的熔沸点取决于共价键的键长和键能,键能越大,键长越短,共价键越强,熔沸点越高。4、常见的原子晶体:(1)某些非金属单质:硼(B)、硅(Si)和锗(Ge)等;(2)某些非金属化合物:二氧化硅、碳化硅(SiC,俗称金刚砂)氮化硼(BN)、氮化硅(Si3N4)①与每个C相邻有个Si,与每个Si相邻有个C,形成空间网状结构晶体,键角。②虚线所示结构单元中,有个共价键,个C,个Si,1molSiC形成molSi—C;SiCSiC的晶体结构的晶体结构1、下列各组物质的晶体中,化学键类型相同,晶体类型也相同的是()A、SO2和SiO2B、CO2和H2OC、NaCl和HClD、CCl4和KCl2、下列叙述正确的是()A.P4和NO2都是共价化合物B.CCl4和NH3都是以极性键结合的极性分子C.在BN和SiO2晶体中都不存在单个小分子3、判断下列说法的正误:ⅰ分子晶体中一定存在范德华力,可能有共价键ⅱ分子晶体中,共价键键能越大,该分子晶体熔沸点一定越高ⅲ分子晶体中,分子间作用力越大,该物质越稳定ⅳ非金属单质都是分子晶体ⅴ分子晶体比原子晶体(如金刚石)的熔沸点低,是因为分子晶体中只存在分子间作用力而不存在化学键ⅵ干冰(固态CO2)升华时,分子内共价键会发生断裂√×××××4、(11年全国)氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN:(5)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有______个氮原子、____个硼原子,立方氮化硼的密度是______________________g·cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。分子晶体、原子晶体结构与性质关系的比较晶体类型分子晶体原子晶体结构粒子间的作用力性质硬度溶、沸点导电溶解性构成晶体粒子分子原子分子间作用力共价键结构、性质较小较大较低很高固态和熔融状态都不导电不导电相似相溶难溶于常见溶剂小结109º28´共价键14×﹕(1/2)=12﹕(2)晶体中最小碳环由不在同一平面的6个C...