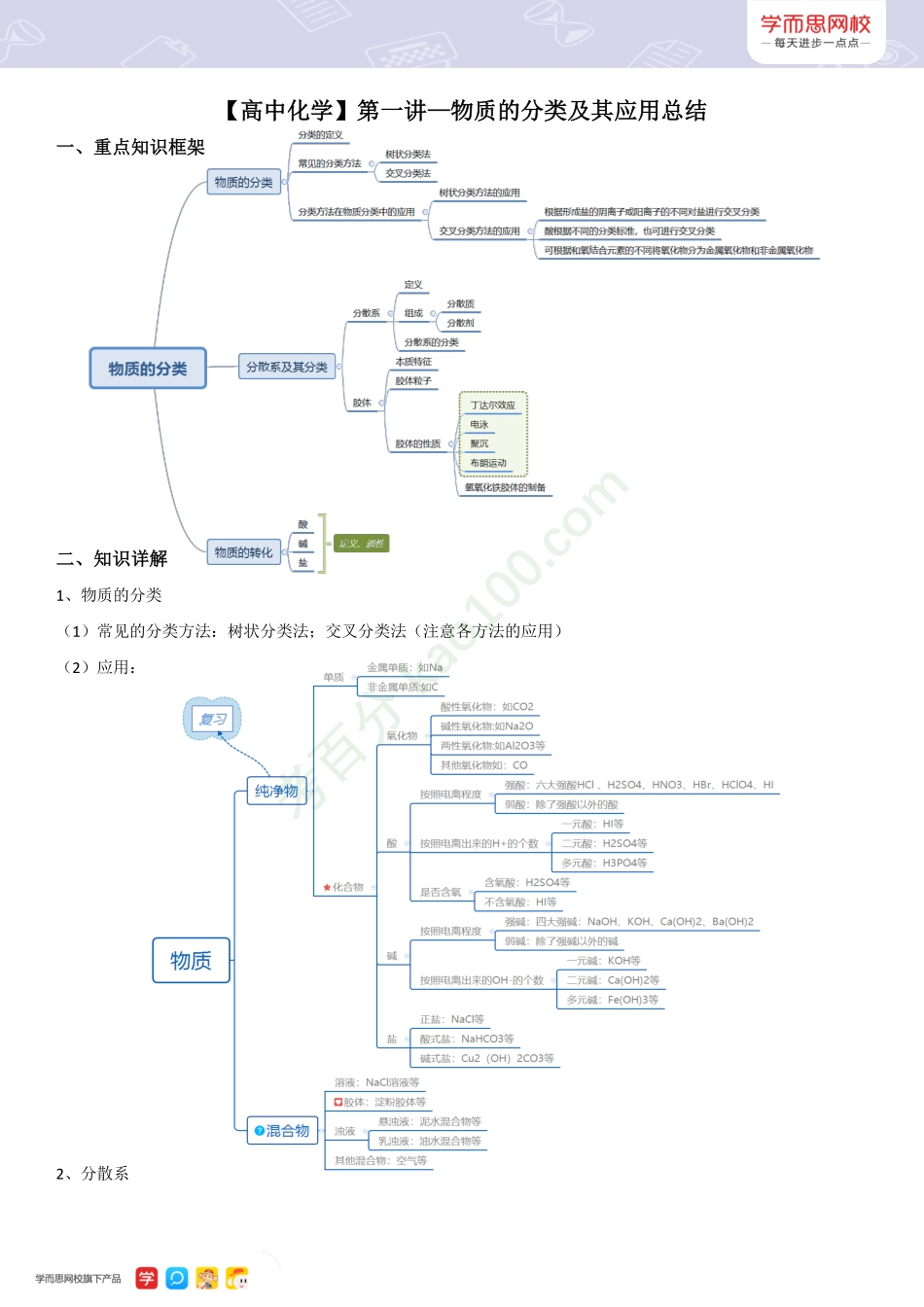
【高中化学】第一讲—物质的分类及其应用总结一、重点知识框架二、知识详解1、物质的分类(1)常见的分类方法:树状分类法;交叉分类法(注意各方法的应用)(2)应用:2、分散系考百分kao100.com(1)定义:一种(或多种)物质分散到另一种(或多种)物质里所得到的体系(2)组成:分散质(被分散成“微粒”的物质);分散剂(容纳分散质的物质)(3)根据分散质粒子的大小分为:溶液、胶体、浊液(悬浊液、乳浊液)3、溶液、胶体和悬浊液的比较分散系溶液胶体悬浊液分散质粒子的直径<1nm1nm~100nm>100nm分散质粒子的组成小分子或离子大分子或分子集合体许多分子的集合体外观均一、透明多均一、透明不均一、不透明稳定性稳定介稳定不稳定分散质能否透过滤纸能能不能分散质能否透过半透膜能不能不能实例食盐水、糖水淀粉胶体、Fe(OH)3胶体泥水4、胶体★(1)性质:丁达尔效应、电泳、聚沉、布朗运动;【注意】胶体不带电,胶体粒子一般带电(2)丁达尔效应定义:光束通过胶体时,形成光亮的通路的现象(用于区分溶液和胶体)★(3)聚沉a.概念:胶体粒子聚集长大,形成颗粒较大的沉淀,从分散剂里析出的现象b.应用:卤水点豆腐、三角洲的形成(4)电泳的应用:血清电泳、静电除尘、冶金工业利用电泳原理选矿,原油脱水等(5)胶体净化的方法:渗析法(将胶体放到半透膜袋中,将其放入水中(或流动的水中),胶体不能透过半透膜,而分子、离子可以透过半透膜,从而可以使杂质离子或者分子进入水中而除去)(6)Fe(OH)3胶体的制备:往一个烧杯里注入蒸馏水5mL,加热至沸腾,然后往沸水里逐滴加入FeCl3饱和溶液5∼6滴,继续煮沸至溶液呈红褐色后,停止加热,得到透明的、红褐色的氢氧化铁胶体;【注意】Fe(OH)3沉淀也为红褐色,如果表明是胶体的话,需要标注清楚;如:Fe(OH)3胶体5、酸、碱、盐的性质(1)酸a.定义:电离产生的阳离子全部都是H+b.性质:与活泼金属发生置换反应;与碱、部分盐发生复分解反应(2)碱a.定义:电离产生的阴离子全部都是OH-b.性质:与酸、部分盐发生复分解反应(3)盐a.定义:电离出金属阳离子或铵根离子和酸根离子b.性质:部分酸、碱发生复分解反应考百分kao100.com