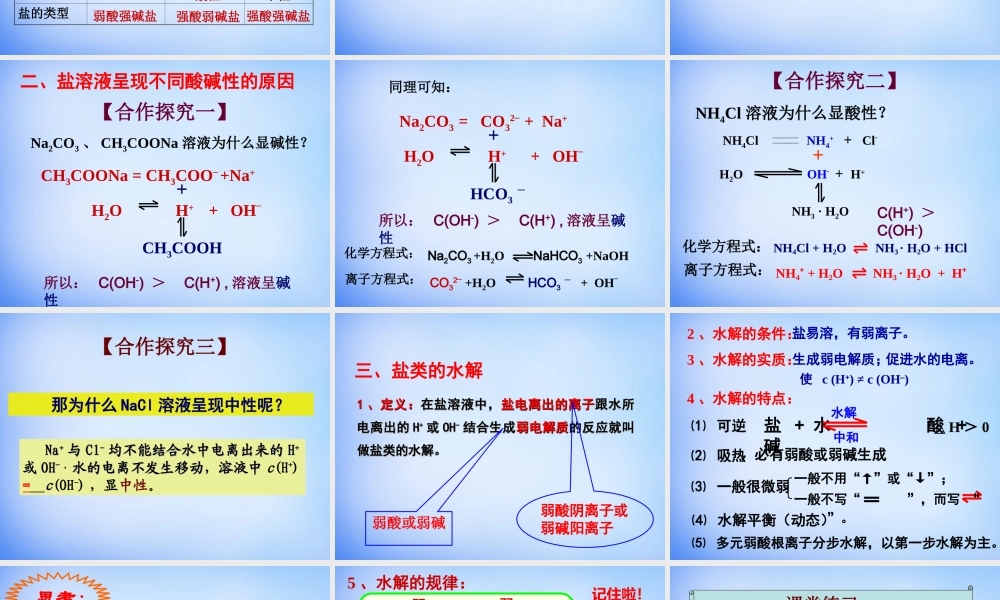
第三章水溶液中的离子平衡第三节盐类的水解•水呈中性,是因为水中的H+的浓度与OH-的浓度相等;•酸呈酸性,是因为酸能够电离出H+而使溶液中的H+的浓度大于OH-的浓度;•碱呈碱性,则是由于碱能够电离出OH-而使溶液中的OH-的浓度大于H+的浓度的缘故。【知识回顾】思考:那盐溶液的酸碱性如何呢,是否一定是呈中性呢?根据形成盐的酸、碱的强弱来分,盐可以分成哪几类?酸+碱==盐+水(中和反应)酸强酸弱酸弱碱强碱碱生成的盐1、强酸强碱盐2、强酸弱碱盐3、强碱弱酸盐4、弱酸弱碱盐NaCl、K2SO4FeCl3、NH4ClCH3COONH4、(NH4)2CO3CH3COONa、K2CO3思考:我们常用什么方法来确定溶液的酸碱性呢?【学生实验】Ⅰ:用PH试纸分别测定CH3COONa、NH4Cl、NaCl、Al2(SO4)3、KNO3溶液的酸碱性。Ⅱ:取1-2ml0.1mol/L的Na2CO3溶液于试管中,向试管中滴入酚酞试液,观察溶液颜色是否变化?一、探究盐溶液的酸碱性的规律【实验记录】>7<7=7溶液CH3COONaNH4ClNaClPH值溶液酸碱性盐的类型碱性酸性中性溶液Na2CO3Al2(SO4)3KNO3PH值溶液酸碱性盐的类型>7<7=7碱性酸性中性弱酸强碱盐强酸弱碱盐强酸强碱盐弱酸强碱盐强酸弱碱盐强酸强碱盐盐溶液酸碱性的规律:【学习反思】谁强显谁性,同强显中性!即:强酸弱碱盐呈酸性弱酸强碱盐呈碱性强酸强碱盐呈中性①NaClO②CaI2③(NH4)2SO4④CuSO4⑤CH3COOK⑥Na2S⑦FeCl3⑧Al(NO3)3⑨CsBr⑩RbF以上溶液中,呈酸性的有,碱性的有,中性的有。【活学活用】③④⑦⑧①⑤⑥⑩②⑨为什么不同的盐溶液会呈现不同酸碱性?【合作探究一】Na2CO3、CH3COONa溶液为什么显碱性?H2OH++OH_CH3COONa=CH3COO_+Na++CH3COOH所以:C(OH-)>C(H+),溶液呈碱性二、盐溶液呈现不同酸碱性的原因H2OH++OH_Na2CO3=CO32_+Na++HCO3-所以:C(OH-)>C(H+),溶液呈碱性同理可知:CO32_+H2OHCO3-+OH_离子方程式:化学方程式:Na2CO3+H2ONaHCO3+NaOH【合作探究二】NH4Cl溶液为什么显酸性?NH4ClNH4++Cl-H2OOH-+H++NH3·H2ONH4Cl+H2ONH3·H2O+HClNH4++H2ONH3·H2O+H+化学方程式:离子方程式:C(H+)>C(OH-)那为什么NaCl溶液呈现中性呢?NaNa++与与ClCl--均不能结合水中电离出来的均不能结合水中电离出来的HH++或或OHOH--,,水的电离不发生移动,溶液中水的电离不发生移动,溶液中c(H+)=c(OH-),显中性。【合作探究三】三、盐类的水解11、定义:、定义:在盐溶液中,在盐溶液中,盐电离出的离子盐电离出的离子跟水所跟水所电离出的电离出的HH++或或OHOH--结合生成结...