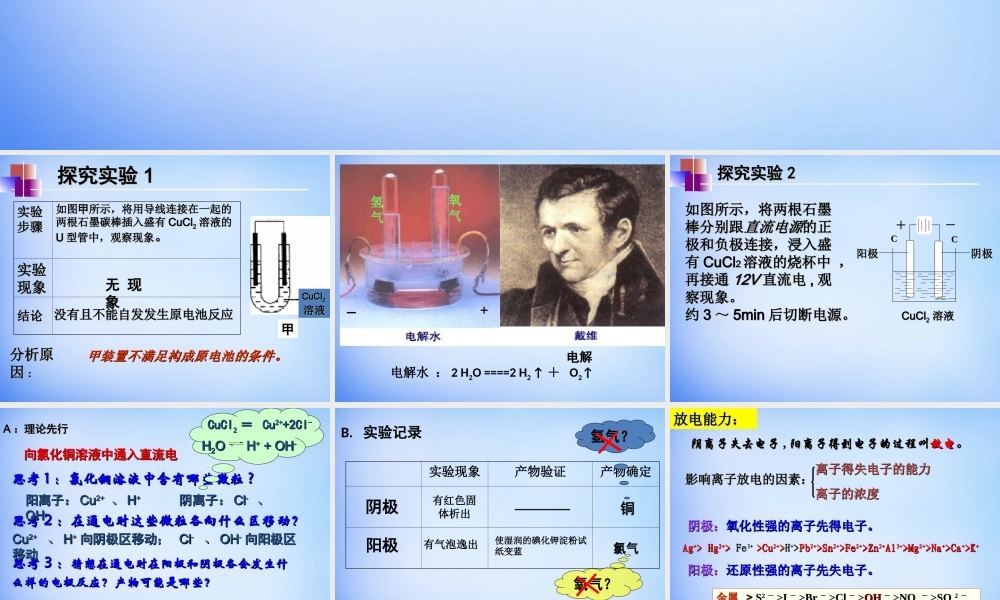
第四章电化学基础第三节电解池探究实验探究实验11甲甲实验实验步骤步骤如图如图甲甲所示,将用导线连接在一起的所示,将用导线连接在一起的两根石墨碳棒插入盛有两根石墨碳棒插入盛有CuClCuCl22溶液的溶液的UU型管中,观察现象型管中,观察现象。。实验实验现象现象结论结论无现无现象象没有且不能自发发生原电池反应没有且不能自发发生原电池反应甲装置不满足构成原电池的条件。甲装置不满足构成原电池的条件。分析原分析原因因::CuClCuCl22溶液溶液氢气氧气电解电解水:2H2O====2H2↑+O2↑+_探究实验探究实验22----如图所示,将两根石墨如图所示,将两根石墨棒分别跟棒分别跟直流电源直流电源的正的正极和负极连接,浸入盛极和负极连接,浸入盛有有CuClCuCl22溶液的烧杯中,溶液的烧杯中,再接通再接通12V12V直流电直流电,,观观察现象。察现象。约约33~~5min5min后切断电源。后切断电源。CCCC阴极阴极阳极阳极CuClCuCl22溶液溶液++--向氯化铜溶液中通入直流电向氯化铜溶液中通入直流电AA:理论先行:理论先行思考思考11:氯化铜溶液中含有哪些微粒:氯化铜溶液中含有哪些微粒??思考思考22:在通电时这些微粒各向什么区移动?:在通电时这些微粒各向什么区移动?思考思考33::猜想在通电时在阳极和阴极各会发生什猜想在通电时在阳极和阴极各会发生什么样的电极反应?产物可能是哪些?么样的电极反应?产物可能是哪些?阳离子:阳离子:CuCu2+2+、、HH++阴离子:阴离子:ClCl--、、OHOH--CuCu2+2+、、HH++向阴极区移动向阴极区移动;;ClCl--、、OHOH--向阳极区向阳极区移动移动ClCl--→Cl→Cl22↑OH↑OH--→O→O22↑↑HH22OHOH+++OH+OH--CuClCuCl22==CuCu2+2++2Cl+2Cl--阴极区:阴极区:CuCu2+2+→CuH→CuH++→H→H22↑↑阳极区:阳极区:B.实验记录实验现象产物验证产物确定有气泡逸出有红色固体析出氯气铜使湿润的碘化钾淀粉试纸变蓝—————氧气?氢气?阴极阳极阴离子失去电子阴离子失去电子,,阳离子得到电子的过程叫阳离子得到电子的过程叫放电放电。。影响离子放电的因素:影响离子放电的因素:离子得失电子的能力离子得失电子的能力离子的浓度离子的浓度放电能力:放电能力:AgAg++>Hg>Hg2+2+>>FeFe3+3+>Cu>Cu2+2+>>HH++>>PbPb2+2+>Sn>Sn2+2+>Fe>Fe2+2+>Zn>Zn2+2+AlAl3+3+>Mg>Mg2+2+>Na>Na++>Ca>Ca++>K>K++阴极:阴极:氧化性强的离子先得电子。氧化性强的离子先得电子。阳极:阳极:还原性强的离子先失电子。还原性强的离...