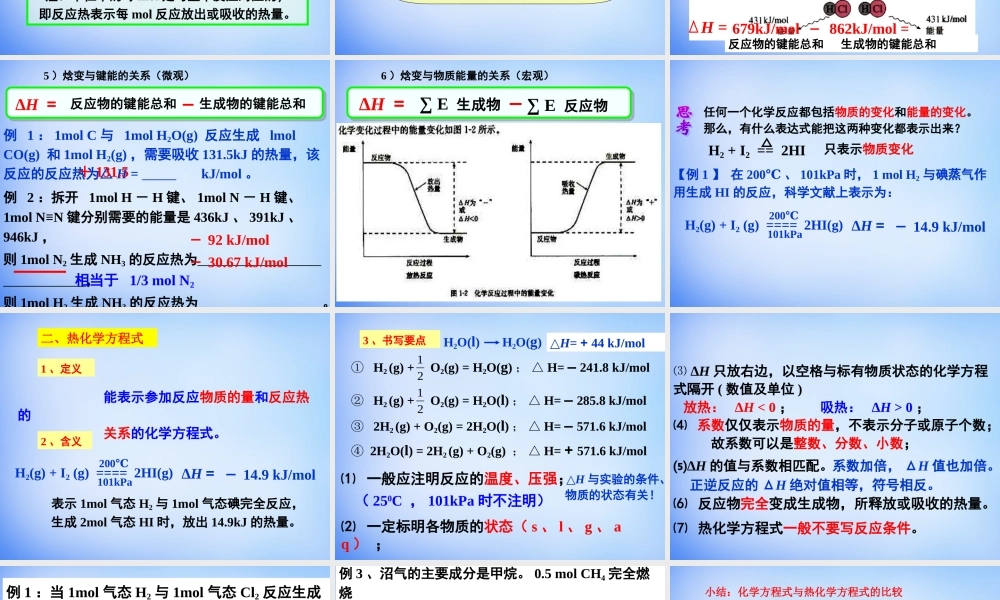
第一章化学反应与能量第一节化学反应与能量的变化1、化学反应的特征物质变化能量变化质量守恒能量守恒2、化学反应中能量的变化(吸收和放出),可以、、及其它形式的能量表现出来。光能热能电能•当能量变化以热能的形式表现时,化学反应可以分为:3、放热反应与吸热反应反高生低生高反低放热反应吸热反应(熟记常见反应)反高(1)放热反应①化学反应中放出热量的反应。②③E(反应物)E(生成物)>生低常见的放热反应:a.物质与O2的氧化反应(燃烧,生锈等);b.中和反应(酸碱);c.金属与水or酸的反应;d.绝大多数化合反应(CaO与H2O)。•C+CO2===2CO吸热反应•放热反应有时也需要加热才能发生!高温生高(2)吸热反应①化学反应中吸收热量的反应。②③E(反应物)E(生成物)<反低常见的吸热反应:a.Ba(OH)2·8H2O晶体与NH4Cl晶体反应;b.H2与CuO等还原反应;c.C作还原剂的反应;d.绝大多数分解反应。C+CO2==2COC+H2O==CO+H2水煤气e.水解反应。一、反应热和焓变1、反应热化学反应中所吸收或放出的热量。恒温恒压下,反应热称“焓变”。2、焓变1)符号:2)单位:ΔHkJ/mol或kJ•mol–1注:单位中的每mol是与整个反应对应的,即反应热表示每mol反应放出或吸收的热量。3)表示方法放热反应(体系能量降低):∆H<0,∆H为“-”吸热反应(体系能量升高):∆H>0,∆H为“+”所谓体系是指被研究的物质系统;而体系以外的其他部分就称为环境4)化学反应中能量变化的原因旧键断裂—吸收能量新键形成—放出能量==679kJ/mol862kJ/molH=679kJ/mol-862kJ/mol=-183kJ/mol反应物的键能总和生成物的键能总和5)焓变与键能的关系(微观)ΔH=反应物的键能总和生成物的键能总和–例1:1molC与1molH2O(g)反应生成lmolCO(g)和1molH2(g),需要吸收131.5kJ的热量,该反应的反应热为△H=kJ/mol。+131.5例2:拆开1molH-H键、1molN-H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则1molN2生成NH3的反应热为,则1molH2生成NH3的反应热为。-92kJ/mol-30.67kJ/mol相当于1/3molN26)焓变与物质能量的关系(宏观)ΔH=∑E生成物∑E反应物–任何一个化学反应都包括物质的变化和能量的变化。那么,有什么表达式能把这两种变化都表示出来?H2+I2==2HI只表示物质变化【例1】在200℃、101kPa时,1molH2与碘蒸气作用生成HI的反应,科学文献上表示为:ΔH=H2(g)+I2(g)====2HI(g)200℃101kPa-14.9kJ/mol二、热化学方程式能表示参加反应物质的量和反应热的关系的化学方程式。1、...