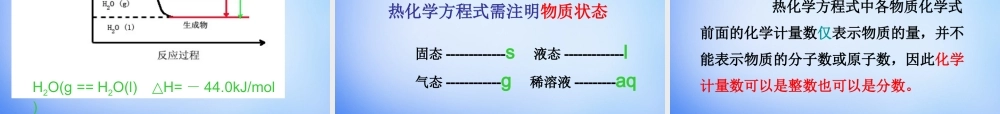
第一章化学反应与能量第一节化学反应与能量的变化化学反应有新物质生成,伴有化学反应有新物质生成,伴有能量变化能量变化,,常表现为热量变化常表现为热量变化((还有光能、电能等还有光能、电能等))。。铁在纯氧中点燃1.常见的放热反应和吸热反应放热反应吸热反应知识回顾大多数化合反应所有燃烧反应酸碱中和反应活泼金属与酸、水反应大多数分解反应H2还原CuOC(s)+H2O(g)Ba(OH)2·8H2O与NH4Cl固体的反应讨论:决定一个化学反应是放热反应还是吸热反应是由条件(如加热)决定吗?请举例说明。反应物的总能量与生成物的总能量的相对大小反应物总能量生成物总能量VS2.引起化学反应中的能量变化的原因:(宏观)由生成物和反应物的焓值差(即焓变)决定。3.各种物质都储存化学能(焓,符号H)能量反应进程反应物生成物焓变反应热(1)化学反应过程中所释放或吸收的热量,叫做反应热。恒压条件下,反应热等于焓变。(2)符号:△H单位:kJ/mol注:单位中的每mol是与整个反应对应的,即反应热表示每mol反应放出或吸收的热量。练习:已知在101kPa时石墨比金刚石稳定。1mol石墨转化为金刚石,要吸收1.895kJ的热能。据此,试判断1mol的石墨与1mol的金刚石所具有的总能量的大小关系如何?HClHClHHHHClClClCl++436kJ/mol243kJ/mol431kJ/mol请你分别计算出H2+Cl2==2HCl吸收和放出的热量是多少?并判断其能量变化?点燃4.引起化学反应中的能量变化的原因:(微观)断开化学键吸收的总能量小于形成化学键释放出的总能量,反应放出能量。能量反应进程断键吸收能量成键释放能量HClClH----释放能量HClClH当∆H为“-”(∆H<0)时,为放热反应当∆H为“+”(∆H>0)时,为吸热反应5.∆H的计算思考一:1molH2与1molCl2反应生成2molHCl释放出184.6kJ的热量,则该反应的△H1=;思考二:已知拆开1molH2中的化学键要吸收436kJ的能量,拆开1molO2中的化学键要吸收496kJ的能量,形成水分子中的1molH—O键要放出463kJ的能量,试说明2H2O===2H2+O2中的能量变化。∆H=生成物的总能量-反应物的总能量∆H=吸收热量总和-放出热量的总和∆H=反应物键能总和-生成物键能总和1.已知反应A+B=C+D为放热反应,对该反应的下列说法中正确的是()A.A的能量一定高于CB.B的能量一定高于DC.A和B的总能量一定高于C和D的总能量D.该反应为放热反应,故不必加热就一定能发生C巩固练习巩固练习11影响焓因素:物质本身性质和状态⑴1gH2O(l)变成水蒸气需要升温还是降温?⑵液态水变成水蒸...