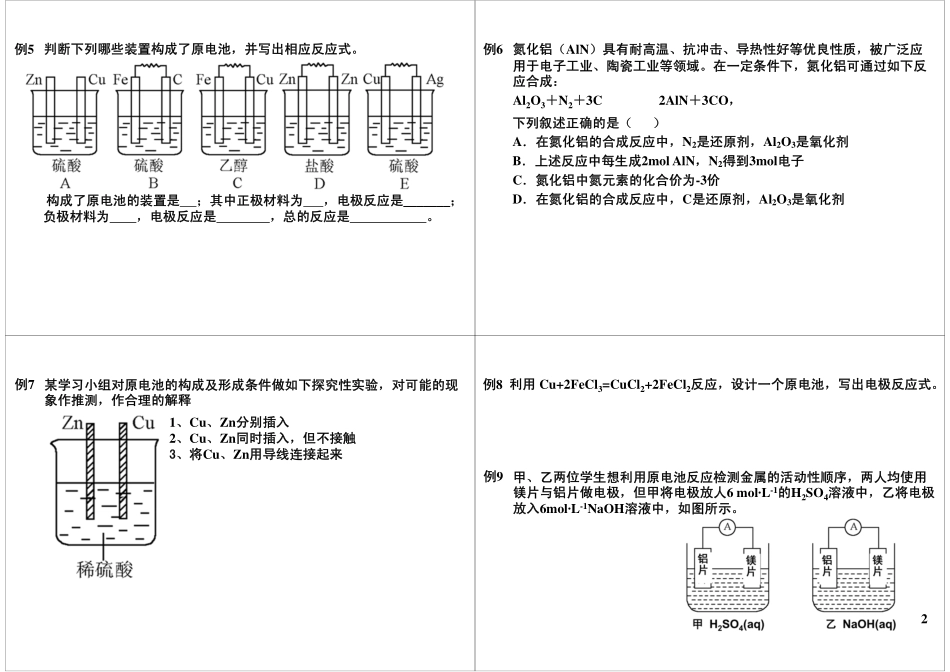
四、电极反应方程式原电池介绍(下)练习:判断是否是原电池,并写出电极方程式例1下列叙述不正确的是()。A.根据一次能源和二次能源的划分,氢气为二次能源B.电能是现代社会中应用最广泛、使用最方便、污染最小的一种二次能源C.火电是将燃料中的化学能直接转化为电能的过程D.在火电过程中,化学能转化为热能的过程中实际上是氧化还原反应发生的过程,伴随着能量的变化例2(1)镁条﹑铜片﹑果汁构成的原电池,负极是________,正极是________;外电路中电子经导线由__________流向_______,电流经导线由_______流向_______。(2)在镁条﹑铁片﹑果汁构成的原电池,负极是______,正极是______,在外电路中电子经导线由_________流向_______,电流经导线由____________流向___________。镁条上发生_________﹙填“氧化”“还原”﹚反应,铁片上发生___________﹙填“氧化”“还原”﹚例3在原电池构成的闭合回路中,关于电子和阴阳离子运动方向的描述正确的是()A.电子从原电池的负极通过导线移动向正极B.电子从原电池的正极通过导线移动向负极C.阴离子在电解质溶液中向正极移动D.阳离子在电解质溶液中向正极移动例4现有A、B、C、D四种金属片,①把A、B用导线连接后同时浸入稀硫酸溶液中,A上有气泡产生;②把C、D用导线连接后同时浸入稀硫酸溶液中,D发生还原反应;③把A、C用导线连接后同时浸入稀硫酸溶液中,电子流动方向为A导线C。根据上述情况,回答下列问题:⑴在①中,金属片发生氧化反应;⑵在②中,金属片作负极;⑶如果把B、D用导线连接后同时浸入稀硫酸溶液,则金属片上有气泡产生;⑷上述四种金属的活动性顺序是。1例5判断下列哪些装置构成了原电池,并写出相应反应式。构成了原电池的装置是;其中正极材料为,电极反应是_______;负极材料为,电极反应是,总的反应是。例6氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C2AlN+3CO,高温下列叙述正确的是()A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂B.上述反应中每生成2molAlN,N2得到3mol电子C.氮化铝中氮元素的化合价为-3价D.在氮化铝的合成反应中,C是还原剂,Al2O3是氧化剂例7某学习小组对原电池的构成及形成条件做如下探究性实验,对可能的现象作推测,作合理的解释1、Cu、Zn分别插入2、Cu、Zn同时插入,但不接触3、将Cu、Zn用导线连接起来4...