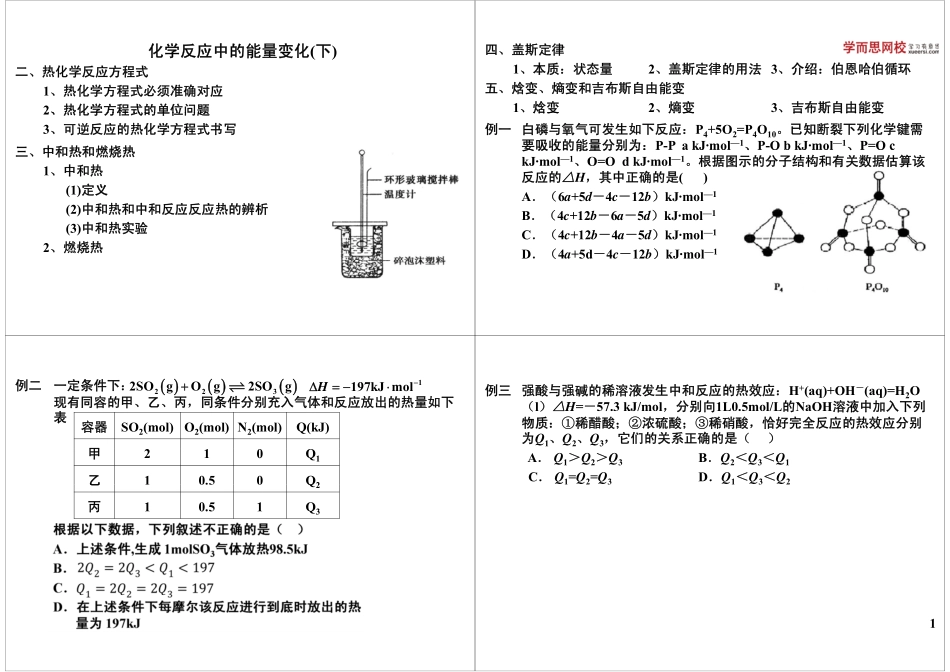
二、热化学反应方程式化学反应中的能量变化(下)、热化学反应方程式1、热化学方程式必须准确对应2、热化学方程式的单位问题2、热化学方程式的单位问题3、可逆反应的热化学方程式书写三中和热和燃烧热三、中和热和燃烧热1、中和热(1)定义(1)定义(2)中和热和中和反应反应热的辨析中和热实验(3)中和热实验2、燃烧热四、盖斯定律1、本质:状态量2、盖斯定律的用法3、介绍:伯恩哈伯循环五、焓变、熵变和吉布斯自由能变1、焓变2、熵变3、吉布斯自由能变焓变熵变吉布斯自由能变例一白磷与氧气可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P-PakJ·mol—1、P-ObkJ·mol—1、P=Oc要吸收的能量分别为:PPakJmol、PObkJmol、POckJ·mol—1、O=OdkJ·mol—1。根据图示的分子结构和有关数据估算该反应的△H,其中正确的是()A.(6a+5d-4c-12b)kJ·mol—1B.(4c+12b-6a-5d)kJ·mol—1C.(4c+12b-4a-5d)kJ·mol—1D.(4a+5d-4c-12b)kJ·mol—1例二一定条件下:现有同容的甲、乙、丙,同条件分别充入气体和反应放出的热量如下表2232SOgOg2SOg1197kJmolH表容器SO2(mol)O2(mol)N2(mol)Q(kJ)甲210Q1乙10.50Q2乙Q2丙10.51Q3例三强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,分别向1L0.5mol/L的NaOH溶液中加入下列(),分别向的溶液中加入下列物质:①稀醋酸;②浓硫酸;③稀硝酸,恰好完全反应的热效应分别为Q1、Q2、Q3,它们的关系正确的是()A.Q1>Q2>Q3B.Q2<Q3<Q1C.Q1=Q2=Q3D.Q1<Q3<Q21例四例五下列关于热化学反应的描述中正确的是()A.HCl和NaOH反应的中和热为△H=-57.3kJ/mol,则H2SO4和24Ca(OH)2反应的中和热△H=2×(-57.3)kJ/molB.CO(g)的燃烧热是283.0kJ/mol,则2molCO常温常压下充分燃烧△H=-2×283.0kJ/molC.需要加热才能发生的反应一定是吸热反应D.甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热例六已知:2CO(g)+O2(g)=2CO2(g)ΔH=-566kJ/molNa2O2(s)+CO2(g)=Na2CO3(s)+1/2O2ΔH=-226kJ/mol根据以上热化学方程式判断,下列说法正确的是()ACO的燃烧热为283kJA.CO的燃烧热为283kJB.上图可表示由CO生成CO2的反应过程和能量关系C2NO()2CO()2NCO()O()ΔH>452kJ/lC.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)ΔH>-452kJ/molD.CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数为6.02×1023例七已知H2(g)+1/2O2(g)=H2O(g)△H11/2N2(g)+O2(g)=NO2(g)△H22(g)2(g)2(g)21/2N2(g)+3/2H2(g)=NH3(g)△H3则2NH3(g)+7/2O2(g)=2NO2(g)+3H2O(g)的△H=()则3(g)2(g)2(g)2(g)的A.2△H1+2△H2-2△H3B.△H1+△H2-△H3B.△H1△H2△H3C.3△H1+2△H2+2△H3D.3△H1+2△H2-2△H3D.3△H1+2△H22△H32