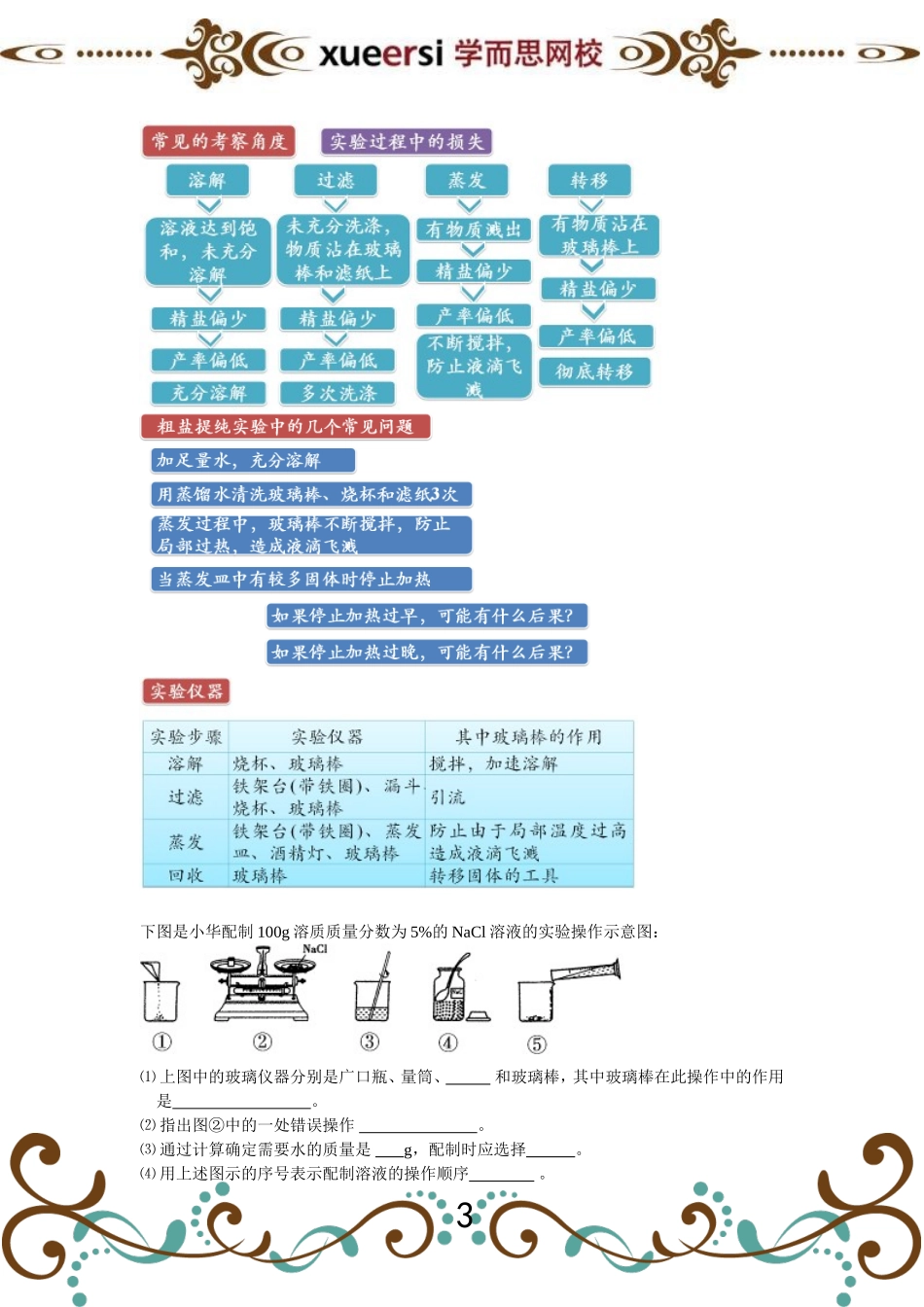
1溶液的配置及粗盐的提纯实验23下图是小华配制100g溶质质量分数为5%的NaCl溶液的实验操作示意图:⑴上图中的玻璃仪器分别是广口瓶、量筒、和玻璃棒,其中玻璃棒在此操作中的作用是。⑵指出图②中的一处错误操作。⑶通过计算确定需要水的质量是g,配制时应选择。⑷用上述图示的序号表示配制溶液的操作顺序。4某中学化学兴趣小组的同学欲通过实验探究,验证粗盐中杂质的种类和NaCl的含量。探究一:这包粗盐中还有什么杂质?提出问题:粗盐中可能含有较多的CaCl2,请你设计实验验证杂质的成分?探究二:这包粗盐中NaCl的质量分数是多少?小凡同学按下面的步骤继续进行了实验,请你帮他补充完整。①称取一定质量的样品(质量为Wg)②将样品加水溶解,制成粗盐溶液③过滤④沉淀洗涤后小心烘干,得到固体A⑤向滤液中滴加适量的稀盐酸后,进行某一操作,即可得到纯净的固体B⑥称量实验中得到的某种固体的质量⑴在②③⑤的步骤中,都使用到一种仪器是,它在步骤②和⑤中的操作方法相同。但目的不同,其目的分别是:⑵步骤⑤进行的“某一操作”是,所需要的主要实验仪器有:⑶步骤⑥中,你认为需称量固体A还是固体B的质量,你不选择称量另一种固体的理由是: