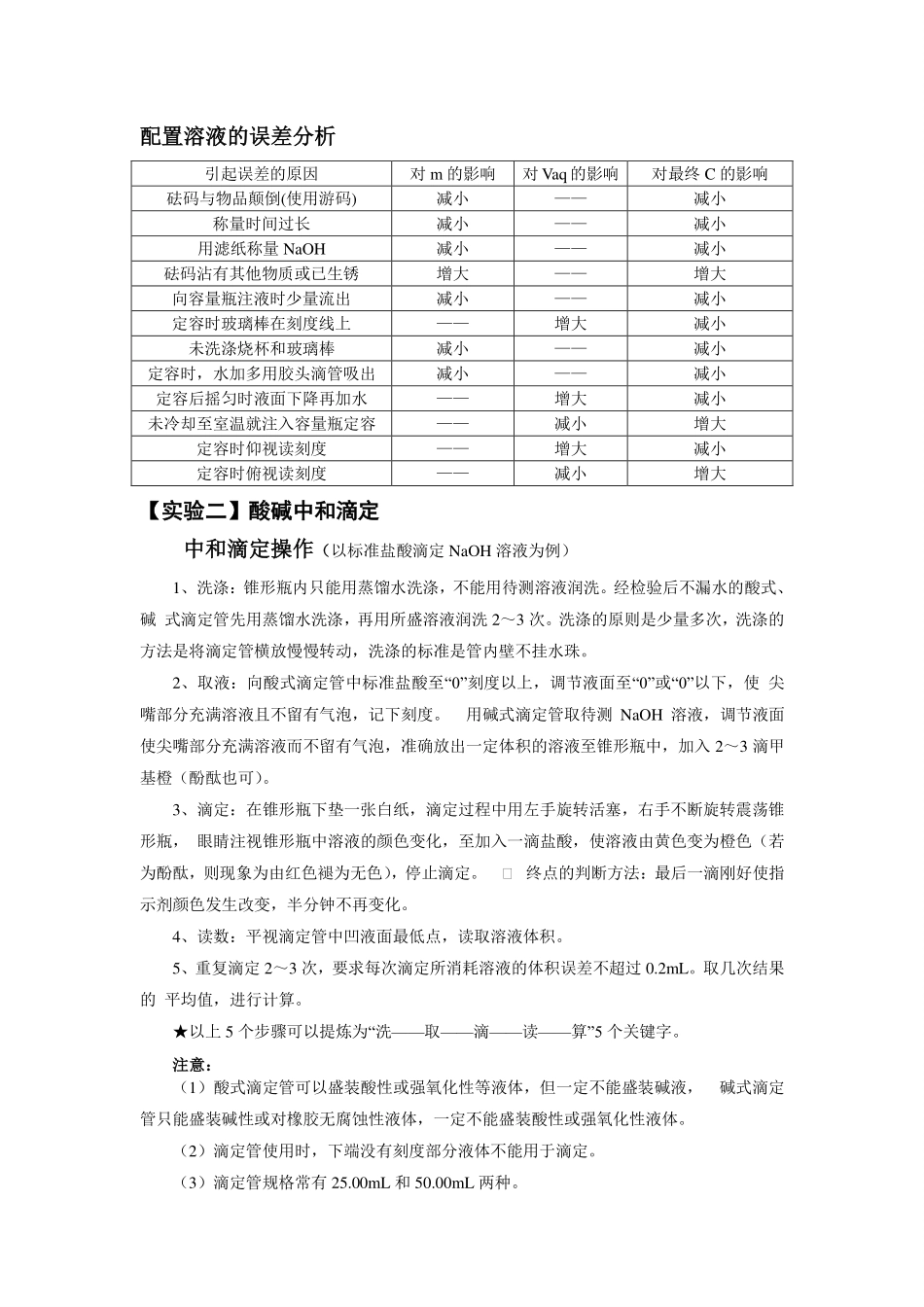
实验中的数值处理【实验一】配置一定浓度溶液(以配置0.2mol/L480mlNaOH为例)配置溶液的步骤①计算:计算所需固体溶质的______或液体溶质的______;②称量或量取:所需仪器:______或______。③溶解或稀释:用水溶解溶质或稀释浓溶液,并冷却到室温。所需仪器:______,______。④转移:将烧杯中的溶液沿______注入______中。⑤洗涤:用蒸馏水洗涤__________________2~3次,并将每次洗涤液都转入______中,振荡,使溶液混合均匀。⑥定容:继续往______中小心地加水,直到液面离______时,改用______滴加蒸馏水至液面与______相切。⑦摇匀:塞好瓶塞,反复上下颠倒,摇匀。容量瓶的使用方法和注意事项(1)查漏容量瓶使用前的第一步操作是检查容量瓶是否漏水。检查方法是:加水→倒立→观察→正立,瓶塞旋转180°→倒立→观察。(2)使用前用蒸馏水洗净,但不能用待配溶液润洗。(3)不能将固体或浓溶液直接在容量瓶中溶解或稀释,容量瓶也不能作为反应容器或长期贮存溶液。(4)容量瓶的容积是在瓶身所标温度下确定的,因而不能将热的溶液转移到容量瓶中。(5)只能配制容量瓶上规定容积的溶液,即不能配制任意体积的一定物质的量浓度的溶液。配置溶液的误差分析【实验二】酸碱中和滴定中和滴定操作(以标准盐酸滴定NaOH溶液为例)1、洗涤:锥形瓶内只能用蒸馏水洗涤,不能用待测溶液润洗。经检验后不漏水的酸式、碱式滴定管先用蒸馏水洗涤,再用所盛溶液润洗2~3次。洗涤的原则是少量多次,洗涤的方法是将滴定管横放慢慢转动,洗涤的标准是管内壁不挂水珠。2、取液:向酸式滴定管中标准盐酸至“0”刻度以上,调节液面至“0”或“0”以下,使尖嘴部分充满溶液且不留有气泡,记下刻度。用碱式滴定管取待测NaOH溶液,调节液面使尖嘴部分充满溶液而不留有气泡,准确放出一定体积的溶液至锥形瓶中,加入2~3滴甲基橙(酚酞也可)。3、滴定:在锥形瓶下垫一张白纸,滴定过程中用左手旋转活塞,右手不断旋转震荡锥形瓶,眼睛注视锥形瓶中溶液的颜色变化,至加入一滴盐酸,使溶液由黄色变为橙色(若为酚酞,则现象为由红色褪为无色),停止滴定。终点的判断方法:最后一滴刚好使指示剂颜色发生改变,半分钟不再变化。4、读数:平视滴定管中凹液面最低点,读取溶液体积。5、重复滴定2~3次,要求每次滴定所消耗溶液的体积误差不超过0.2mL。取几次结果的平均值,进行计算。★以上5个步骤可以提炼为“洗——取——滴——读——算”5个关键字。注意:(1)酸式滴定管...