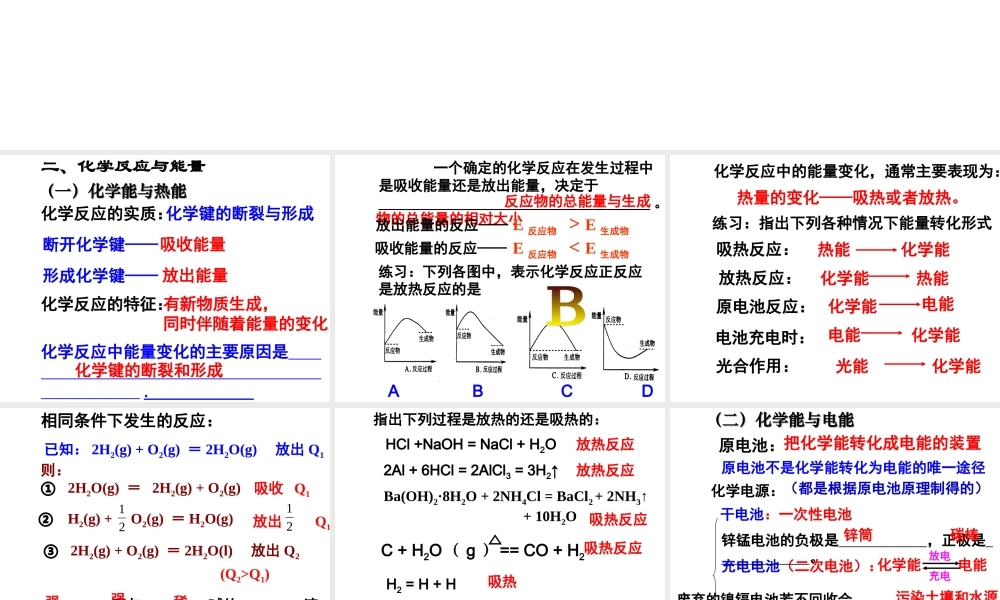
《第二章化学反应与能量》知识点梳理(一)(一)化学能与热能化学能与热能二、化学反应与能量断开化学键——吸收能量形成化学键——放出能量化学反应中能量变化的主要原因是.化学键的断裂和形成化学反应的特征:有新物质生成,同时伴随着能量的变化化学键的断裂与形成化学反应的实质:一个确定的化学反应在发生过程中是吸收能量还是放出能量,决定于_____________________________________。反应物的总能量与生成物的总能量的相对大小放出能量的反应——E反应物>E生成物吸收能量的反应——E反应物Q1)酸与碱的溶液发生中和反应生成时所释放的热量称为中和热1molH2O强强稀指出下列过程是放热的还是吸热的:HCl+NaOH=NaCl+H2O放热反应2Al+6HCl=2AlCl3=3H2↑放热反应Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O吸热反应C+H2O(g)==CO+H2吸热反应H2=H+H吸热2Na2O2+2CO2=2Na2CO3+O2放热反应(二)(二)化学能与电能化学能与电能原电池:把化学能转化成电能的装置原电池不是化学能转化为电能的唯一途径化学电源:(都是根据原电池原理制得的)干电池:一次性电池充电电池(二次电池):燃料电池:锌锰电池的负极是,正极是。锌筒碳棒化学能电能放电充电废弃的镍镉电池若不回收会污染土壤和水源是一种高效、环境友好的发电装置原电池的构成条件:一电解质溶液、一个自发的氧化还原反应、形成闭合回路两个电极、CuFe酒精FeCuSO4溶液Cu下列装置中,能构成原电池的是:ZnH2SO4溶液CZnZnH2SO4溶液CFe醋酸溶液CuCuSO4溶液Fe稀H2SO4ABCDEF√√练习:将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是A.两烧杯中铜片表面均无气泡产生B.甲中铜片是正极,乙中铜片是负极C.两烧杯中溶液的pH值均增大D.产生气泡的速度甲比乙慢ZnCuZnCu稀硫酸甲乙原电池负极的本质特征:失去电子原电池负极的判断:相对活泼的金属;失去电子,作还原剂;元素化合价升高;被氧化;发生氧化反应;电子流出...