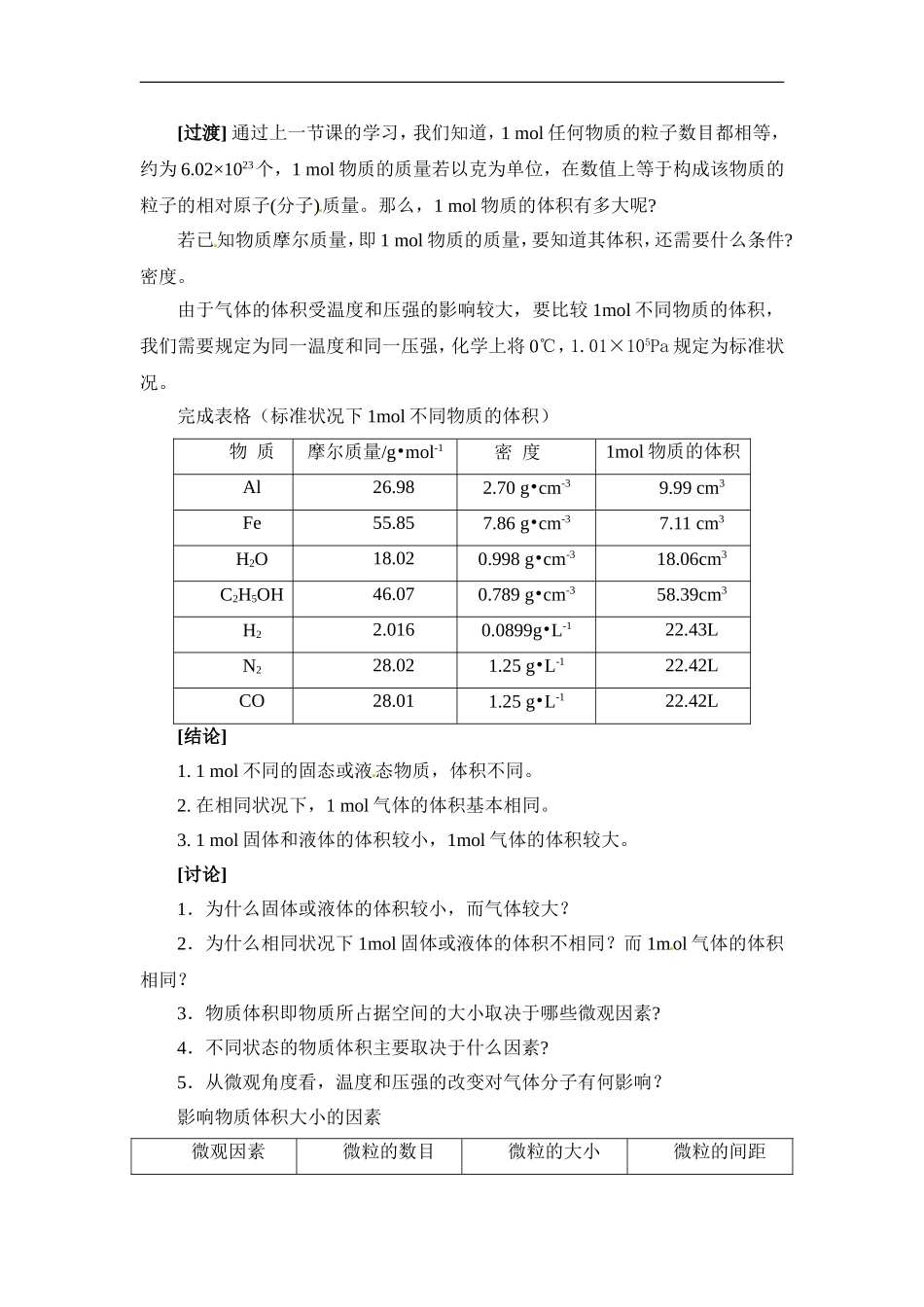
第1单元课时3物质的聚集状态教学设计一、学习目标1.知道不同聚集状态物质的一些特性,根据物质的存在状态进行分类,知道固、液、气态物质的一些特性。2.了解影响气体体积的主要因素,初步学会运用气体摩尔体积等概念进行简单的计算。3.引导学生从微观角度理解化学物质的存在状态,在原有基础上提升对化学物质的认识,同时为后续内容的学习打好必要的基础。二、教学重点及难点理解气体摩尔体积等概念并进行简单的计算三、设计思路本课时设计先从学生熟悉的“三态”这一宏观特征引入,探究影响物质体积的微观原因,让学生体验从宏观到微观的研究方法,从而引出“气体摩尔体积”的概念,通过一定的讨论、辨析,初步理解“气体摩尔体积”这一重要概念。四、教学过程[导入]日常生活中接触到的物质丰富多彩,例如自由流动的空气、香气扑鼻的咖啡、晶莹剔透的水晶等等。这些物质都是由大量原子、分子、离子等微观粒子聚集在一起构成的。物质有哪些常见的聚集状态呢?气态、液态和固态。不同状态的物质物理性质上有哪些差异?固体有固定的形状,液体没有固定的形状,但有固定的体积,气体没有固定的形状和体积;气体容易被压缩,而固体液体不易被压缩。为什么固态、液态和气态物质之间存在这些差异?如何解释这种差异呢?结构决定性质。指导学生阅读、分析教材表1-3,形成认识:由于微观结构上的差异,三种不同聚集状态的物质各有独特的性质。[过渡]通过上一节课的学习,我们知道,1mol任何物质的粒子数目都相等,约为6.02×1023个,1mol物质的质量若以克为单位,在数值上等于构成该物质的粒子的相对原子(分子)质量。那么,1mol物质的体积有多大呢?若已知物质摩尔质量,即1mol物质的质量,要知道其体积,还需要什么条件?密度。由于气体的体积受温度和压强的影响较大,要比较1mol不同物质的体积,我们需要规定为同一温度和同一压强,化学上将0℃,1.01×105Pa规定为标准状况。完成表格(标准状况下1mol不同物质的体积)物质摩尔质量/g•mol-1密度[来源:学科网]1mol物质的体积Al26.982.70g•cm-39.99cm3Fe55.857.86g•cm-37.11cm3H2O18.020.998g•cm-318.06cm3C2H5OH46.070.789g•cm-358.39cm3H22.0160.0899g•L-122.43LN228.021.25g•L-122.42LCO28.011.25g•L-122.42L[结论]1.1mol不同的固态或液态物质,体积不同。2.在相同状况下,1mol气体的体积基本相同。3.1mol固体和液体的体积较小,1mol气体的体积较大。[讨论]1.为什么固体或液体的体积较小,而气体...