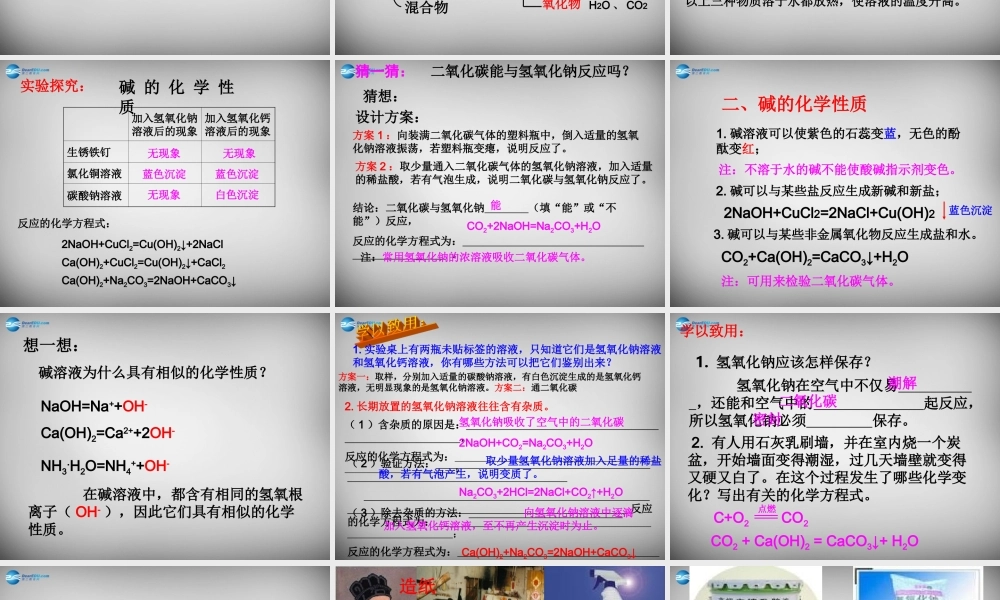
第二节碱及其性质常见的碱:二、碱的性质氢氧化钠氢氧化钙氢氧化钾氨水NaOHCa(OH)2KOHNH3·H2O性质氢氧化钠氢氧化钙颜色、状态在水中的溶解性露置于空气中的变化其他俗称微溶于水(石灰水)腐蚀性强腐蚀性易溶于水(放出大量的热)白色固体苛性钠、火碱、烧碱白色粉末熟石灰、消石灰易吸水而潮解…不潮解,易与CO2反应而变质一、常见的碱:1、NaOH和Ca(OH)2的物理性质(可做干燥剂)(密封保存)现象:剧烈反应,放出大量的热。CaCO3CaO+CO2↑高温生石灰熟石灰3.氧化钙(生石灰)的制法。2.Ca(OH)2的制法:CaO+H2O=Ca(OH)2注意:氧化钙(生石灰)可以做干燥剂思考:1、物质的分类2、哪些物质可做干燥剂?物质纯净物混合物单质化合物酸碱盐氧化物HCI、H2SO4、HNO3NaOH、Ca(OH)2、KOHNaCI、Na2SO4H2O、CO2干燥剂浓硫酸氢氧化钠固体氧化钙以上三种物质溶于水都放热,使溶液的温度升高。实验探究:碱的化学性质加入氢氧化钠溶液后的现象加入氢氧化钙溶液后的现象生锈铁钉氯化铜溶液碳酸钠溶液无现象无现象蓝色沉淀蓝色沉淀无现象白色沉淀反应的化学方程式:2NaOH+CuCl2=Cu(OH)2↓+2NaClCa(OH)2+CuCl2=Cu(OH)2↓+CaCl2Ca(OH)2+Na2CO3=2NaOH+CaCO3↓猜一猜:二氧化碳能与氢氧化钠反应吗?猜想:设计方案:方案1:向装满二氧化碳气体的塑料瓶中,倒入适量的氢氧化钠溶液振荡,若塑料瓶变瘪,说明反应了。方案2:取少量通入二氧化碳气体的氢氧化钠溶液,加入适量的稀盐酸,若有气泡生成,说明二氧化碳与氢氧化钠反应了。结论:二氧化碳与氢氧化钠(填“能”或“不能”)反应,反应的化学方程式为:。能CO2+2NaOH=Na2CO3+H2O注:常用氢氧化钠的浓溶液吸收二氧化碳气体。1.碱溶液可以使紫色的石蕊变蓝,无色的酚酞变红;2.碱可以与某些盐反应生成新碱和新盐;3.碱可以与某些非金属氧化物反应生成盐和水。CO2+Ca(OH)2=CaCO3↓+H2O注:不溶于水的碱不能使酸碱指示剂变色。注:可用来检验二氧化碳气体。二、碱的化学性质2NaOH+CuCl2=2NaCl+Cu(OH)2蓝色沉淀想一想:碱溶液为什么具有相似的化学性质?NaOH=Na++OH-Ca(OH)2=Ca2++2OH-NH3.H2O=NH4++OH-在碱溶液中,都含有相同的氢氧根离子(OH-),因此它们具有相似的化学性质。1.实验桌上有两瓶未贴标签的溶液,只知道它们是氢氧化钠溶液和氢氧化钙溶液,你有哪些方法可以把它们鉴别出来?方案一:取样,分别加入适量的碳酸钠溶液,有白色沉淀生成的是氢氧化钙溶液,无明显现象的是氢氧化钠溶液。方案二:通二氧化碳2....