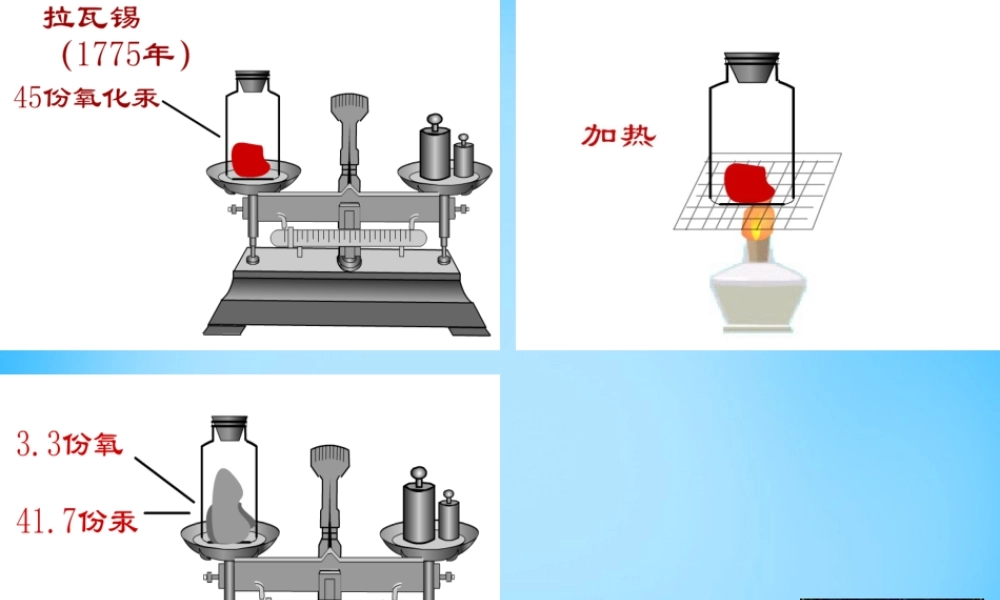
§5-1质量守恒定律提出问题:总和化学反应前后,物质的质量会怎样变化呢?作出假设:生成物的质量总和反应物的质量总和等于等于大于大于小于小于化学反应前后请注意观察以下实验中反应物、生成物的状态及其它变化现象,记录实验中观察到的质量变化情况实验1小结:M1M1M2M2现象:质量:产生大量白烟,放热,气球先膨胀后缩小。==点燃磷(固)+氧气(气)五氧化二磷(固)实验2小结:铁(固)+硫酸铜(液)→铜(固)+硫酸亚铁(液)M1M2现象:铁钉表面变成红色,溶液由蓝色变成浅绿色质量:=得出结论:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和,这个规律就叫质量守恒定律。在敞口容器中:盐酸(液)+碳酸钠(固)→氯化钠(固)+水(液)+二氧碳(气)M1M2>盐酸(液)+碳酸钠(固)→氯化钠(固)+水(液)+二氧化碳(气)M1M2在密闭容器中==在密闭容器中镁(固)+氧气(气)→氧化镁(固)M1M2点燃为了验证化学反应必然遵循质量守恒定律:对于有气体参加或有气体生成化学反应,必须在密闭容器中进行。以氢气在氧气中燃烧生成水为例,分析化学反应中分子、原子种类、数目和质量的变化情况,并由此说明化学反应为什么一定符合质量守恒定律。讨论原子数目原子质量原子种类微观元素质量元素种类一定不变一定不变物质的种类分子的种类一定改变可能改变分子数目宏观质量守恒定律的简单应用.1、6g的碳在充足的氧气中燃烧,生成二氧化碳22g,则有____g的氧气参加反应。163、在化学反应2XY2+Y2=2Z中Z的化学式为()A、X2Y3B、XY3C、X2Y6D、X2Y42、已知石蜡是蜡烛的主要成分,蜡烛在空气中完全燃烧后的产物是CO2和H2O,判断石蜡中一定含有_______元素,可能含有___元素。C、HOB4、高锰酸钾完全分解后,称量剩余固体的质量,比高锰酸钾的质量小。因此这个反应不遵守质量守恒定律。你认可这种说法吗?为什么?根据质量守恒定律,化学反应前高锰酸钾的质量等于生成的锰酸钾、二氧化锰和氧气的质量总和,氧气扩散到空气中,所以剩余固体质量减小。不认可。谢谢!