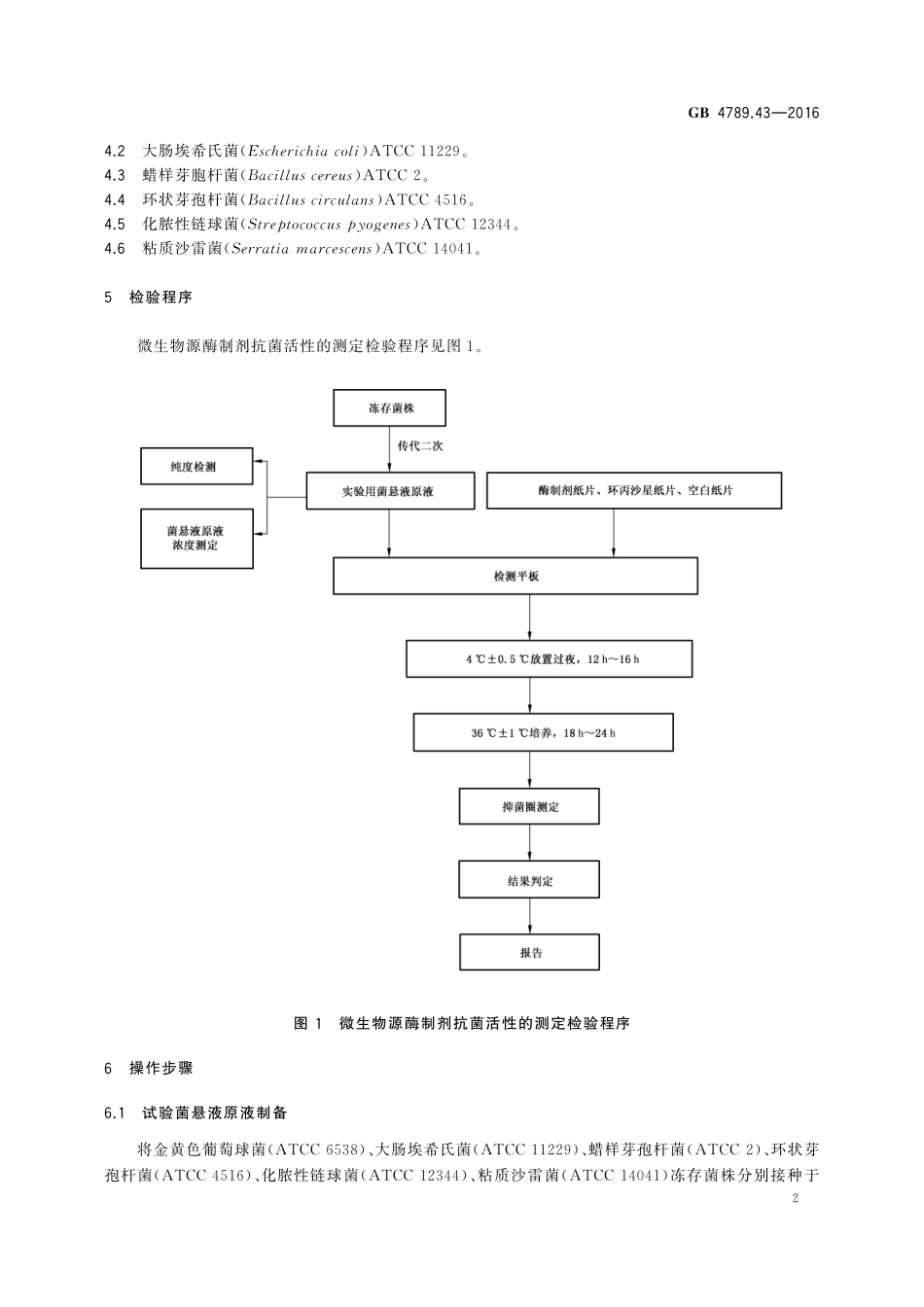
中华人民共和国国家标准GB4789.43—2016食品安全国家标准食品微生物学检验微生物源酶制剂抗菌活性的测定2016-12-23发布2017-06-23实施中华人民共和国国家卫生和计划生育委员会国家食品药品监督管理总局发布GB4789.43—20161食品安全国家标准食品微生物学检验微生物源酶制剂抗菌活性的测定1范围本标准规定了微生物源酶制剂抗菌活性的测定方法。本标准适用于用微生物生产的酶制剂抗菌活性的测定。2设备和材料除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:2.1生物安全柜。2.2冰箱:2℃~5℃。2.3恒温培养箱:36℃±1℃。2.4恒温水浴箱:46℃±1℃。2.5天平:感量为0.1g。2.6振荡器。2.7无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或微量移液器及吸头。2.8无菌培养皿:直径90mm。2.9无菌锥形瓶:容量250mL、500mL。2.10pH计或精密pH试纸。2.11无菌纸片:见A.8。2.12无菌镊子。2.13游标卡尺:刻度为0.1mm。3培养基和试剂3.1胰蛋白胨大豆琼脂(TryptoneSoyAgar,TSA):见A.1。3.2胰蛋白胨大豆肉汤(TryptoneSoyBroth,TSB):见A.2。3.3平板计数琼脂(PlateCountAgar):见A.3。3.40.1mol/LHCl:见A.4。3.5无菌生理盐水:见A.5。3.650.0μg/mL环丙沙星(Ciprofloxacin,CIP)溶液:见A.6。3.75.0μg/片环丙沙星纸片:见A.7。4试验菌株4.1金黄色葡萄球菌(Staphylococcusaureus)ATCC6538。GB4789.43—201624.2大肠埃希氏菌(Escherichiacoli)ATCC11229。4.3蜡样芽胞杆菌(Bacilluscereus)ATCC2。4.4环状芽孢杆菌(Bacilluscirculans)ATCC4516。4.5化脓性链球菌(Streptococcuspyogenes)ATCC12344。4.6粘质沙雷菌(Serratiamarcescens)ATCC14041。5检验程序微生物源酶制剂抗菌活性的测定检验程序见图1。图1微生物源酶制剂抗菌活性的测定检验程序6操作步骤6.1试验菌悬液原液制备将金黄色葡萄球菌(ATCC6538)、大肠埃希氏菌(ATCC11229)、蜡样芽孢杆菌(ATCC2)、环状芽孢杆菌(ATCC4516)、化脓性链球菌(ATCC12344)、粘质沙雷菌(ATCC14041)冻存菌株分别接种于GB4789.43—20163盛有5mLTSB的试管,置36℃±1℃培养18h~24h进行第一次传代培养,分别挑取第一次传代培养液1~2环转种于5mLTSB肉汤,置36℃±1℃培养18h~24h进行二次传代培养,作为试验菌悬液原液备用。试验菌悬液原液纯度检测:分别挑取试验菌悬液原液各一环,划线接种于TSA平板,36℃±1℃培养20h~24h,观察纯度。6.2菌悬液原液浓度测定6.2.1菌悬液原液稀释分别取6.1中制备的菌悬液原液依次进行十倍梯度稀释,蜡样芽孢杆菌和环状芽孢...