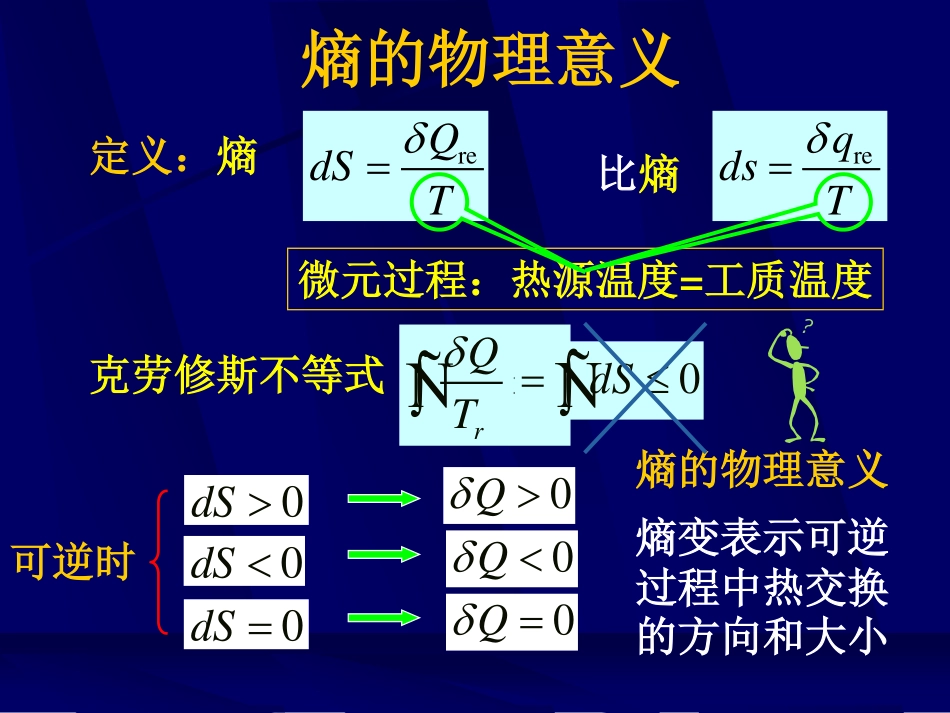
熵的物理意义定义:熵reQdST微元过程:热源温度=工质温度比熵reqdsT0rQTÑ克劳修斯不等式0dS0Q0dS0Q0dS可逆时0Q熵变表示可逆过程中热交换的方向和大小熵的物理意义0dSÑ熵是状态量可逆循环0dSÑ0QTÑpv12ab12210abQQTT2112bbQQTT1212abQQTT1212abSS熵变与路径无关,只与初终态有关0dSdS可逆不可逆ÑÑ2121SS可逆不可逆Entropychange不可逆过程S与传热量的关系12210abQQTT212112QSSST任意不可逆循环0QTÑ2112bbQQTT211212abQQSTTpv12ab=可逆>不可逆S与传热量的关系212112QSSST=可逆>不可逆<不可能热二律表达式之一对于循环克劳修斯不等式QST除了传热,还有其它因素影响熵不可逆绝热过程0dS0Q不可逆因素会引起熵变化=0总是熵增针对过程熵流和熵产对于任意微元过程有:=:可逆过程>:不可逆过程定义fQdST熵产:纯粹由不可逆因素引起g0dSgfdSdSdS结论:熵产是过程不可逆性大小的度量。QdST熵流:永远fgSSS热二律表达式之一EntropyflowandEntropygeneration熵流、熵产和熵变(闭口系统)任意不可逆过程gfdSdSdSfgSSS0Sf0Sg0S可逆过程f0SSg0S不可逆绝热过程0Sf0Sg0S可逆绝热过程0Sf0Sg0S不易求熵变的计算方法理想气体2221v11lndTvScRTv仅可逆过程适用2221p11lndTpScRTp2221pv11dvdpSccvpTs1234132131231QSSST242141242QSSST任何过程熵变的计算方法非理想气体:查图表固体和液体:通常pvccc常数例:水4.1868kJ/kg.KcreQdUpdvdUcmdT熵变与过程无关,假定可逆:reQcmdTdSTT21lnTScmT熵变的计算方法热源(蓄热器):与外界交换热量,T几乎不变假想蓄热器RQ1Q2WT2T1T111QST热源的熵变熵变的计算方法功源(蓄功器):与只外界交换功0S功源的熵变理想弹簧无耗散§5-5孤立系统熵增原理孤立系统0fdS无质量交换0gisodSdS结论:孤立系统的熵只能增大,或者不变,绝不能减小,这一规律称为孤立系统熵增原理。无热量交换无功量交换=:可逆过程>:不可逆过程热二律表达式之一为什么用孤立系统?孤立系统=非孤立系统+相关外界iso0dS=:可逆过程reversible>:不可逆过程irre...