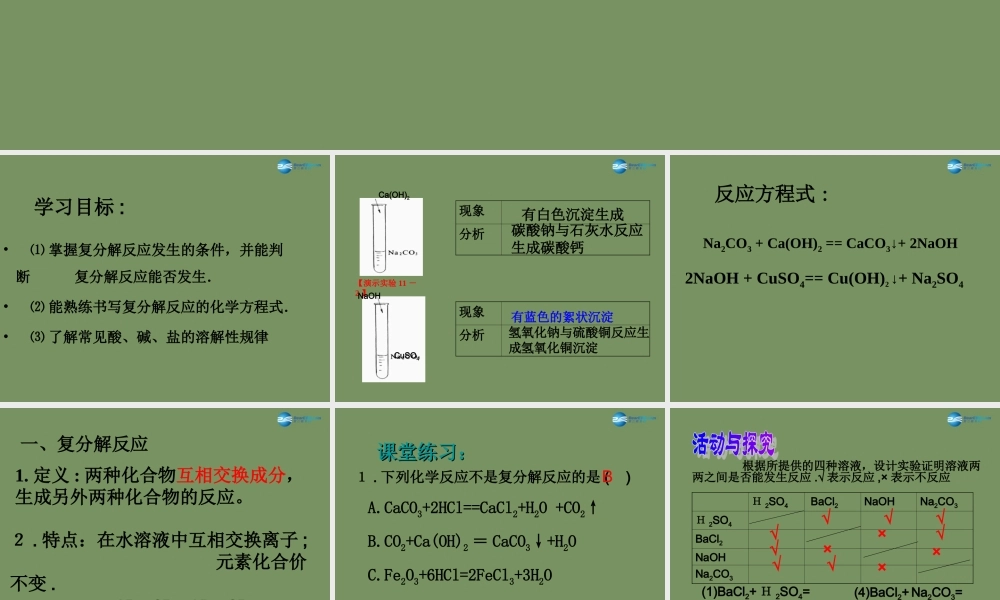
课题2生活中常见的盐(第2课时)探究复分解反应及发生的条件学习目标:•⑴掌握复分解反应发生的条件,并能判断复分解反应能否发生.•⑵能熟练书写复分解反应的化学方程式.•⑶了解常见酸、碱、盐的溶解性规律【演示实验11-2】现象分析有白色沉淀生成碳酸钠与石灰水反应生成碳酸钙现象分析CuSO4NaOHCa(OH)2有蓝色的絮状沉淀氢氧化钠与硫酸铜反应生成氢氧化铜沉淀反应方程式:Na2CO3+Ca(OH)2==CaCO3↓+2NaOH2NaOH+CuSO4==Cu(OH)2↓+Na2SO4一、复分解反应1.定义:两种化合物互相交换成分,生成另外两种化合物的反应。2.特点:在水溶液中互相交换离子;元素化合价不变.AB+CD=AD+CB课堂练习:课堂练习:1.下列化学反应不是复分解反应的是()A.CaCO3+2HCl==CaCl2+H2O+CO2↑B.CO2+Ca(OH)2=CaCO3↓+H2OC.Fe2O3+6HCl=2FeCl3+3H2OD.NaOH+HNO3=NaNO3+H2OB根据所提供的四种溶液,设计实验证明溶液两两之间是否能发生反应.√表示反应,×表示不反应H2SO4BaCl2NaOHNa2CO3H2SO4BaCl2NaOHNa2CO3(1)BaCl2+H2SO4=(2)NaOH+H2SO4=(3)Na2CO3+H2SO4=(4)BaCl2+Na2CO3=(5)BaCl2+NaOH=(6)Na2CO3+NaOH=√√√√√√√√××××实验现象及结论:BaCl2+H2SO4=BaSO4+2HCl2NaOH+H2SO4=Na2SO4+2H2ONa2CO3+H2SO4=Na2SO4+H2O+CO2BaCl2+Na2CO3=BaCO3+2NaClBaCl2+NaOH=不反应Na2CO3+NaOH=不反应有白色沉淀生成有水生成有气体生成有白色沉淀生成3.复分解发生反应的条件两种化合物交换成分时,必需有沉淀或气体或水生成。物质溶解性口诀:物质溶解性口诀:酸都溶。酸都溶。钾、钠、铵、硝盐全溶。钾、钠、铵、硝盐全溶。碱溶钾、钠、钡、铵、钙微溶。碱溶钾、钠、钡、铵、钙微溶。碳酸盐只溶钾、钠、铵、剩下都不溶碳酸盐只溶钾、钠、铵、剩下都不溶氯化银氯化银,,硫酸钡既不溶于水又不溶于酸硫酸钡既不溶于水又不溶于酸OH-NO3-Cl-SO42-CO32-H+溶、挥溶、挥溶溶、挥NH4+溶、挥溶溶溶溶K+溶溶溶溶溶Na+溶溶溶溶溶Ba2+溶溶溶不不Ca2+微溶溶微不Mg2+不溶溶溶微Al3+不溶溶溶——Mn2+不溶溶溶不Zn2+不溶溶溶不Fe2+不溶溶溶不Fe3+不溶溶溶——Cu2+不溶溶溶不Ag+——溶不微不酸、碱、盐的溶解性(20℃)红褐色蓝色2.判断下列复分解反应能发生的写出化学方程式,不能反应的说明理由(1)Ca(OH)2+HCl─(2)NaCl+HNO3─(3)CuCl2+NaOH─(4)CaCO3+Ba(OH)2─(5)AgNO3+KCl─(6)Cu(OH)2+K2CO3─课堂练习:课堂练习:3.下列各组物质的溶液混合后,不能发生反应的是()A.Na2CO3和H2SO4B.NaOH和HClC.NaC...