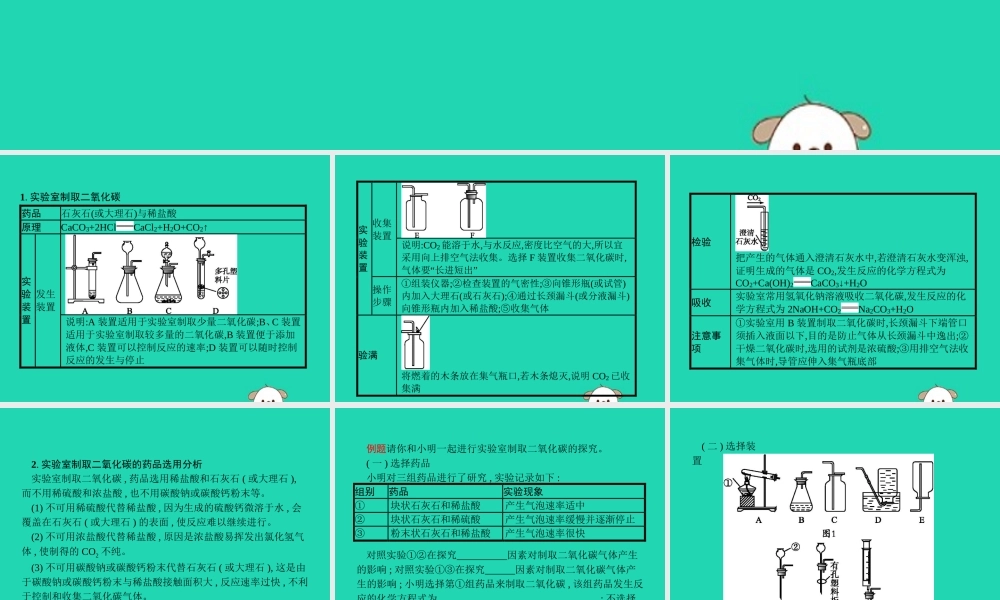
实验二氧化碳的实验室制取1.实验室制取二氧化碳药品石灰石(或大理石)与稀盐酸原理CaCO3+2HClCaCl2+H2O+CO2↑实验装置发生装置说明:A装置适用于实验室制取少量二氧化碳;B、C装置适用于实验室制取较多量的二氧化碳,B装置便于添加液体,C装置可以控制反应的速率;D装置可以随时控制反应的发生与停止实验装置收集装置说明:CO2能溶于水,与水反应,密度比空气的大,所以宜采用向上排空气法收集。选择F装置收集二氧化碳时,气体要“长进短出”操作步骤①组装仪器;②检查装置的气密性;③向锥形瓶(或试管)内加入大理石(或石灰石);④通过长颈漏斗(或分液漏斗)向锥形瓶内加入稀盐酸;⑤收集气体验满将燃着的木条放在集气瓶口,若木条熄灭,说明CO2已收集满检验把产生的气体通入澄清石灰水中,若澄清石灰水变浑浊,证明生成的气体是CO2,发生反应的化学方程式为CO2+Ca(OH)2CaCO3↓+H2O吸收实验室常用氢氧化钠溶液吸收二氧化碳,发生反应的化学方程式为2NaOH+CO2Na2CO3+H2O注意事项①实验室用B装置制取二氧化碳时,长颈漏斗下端管口须插入液面以下,目的是防止气体从长颈漏斗中逸出;②干燥二氧化碳时,选用的试剂是浓硫酸;③用排空气法收集气体时,导管应伸入集气瓶底部2.实验室制取二氧化碳的药品选用分析实验室制取二氧化碳,药品选用稀盐酸和石灰石(或大理石),而不用稀硫酸和浓盐酸,也不用碳酸钠或碳酸钙粉末等。(1)不可用稀硫酸代替稀盐酸,因为生成的硫酸钙微溶于水,会覆盖在石灰石(或大理石)的表面,使反应难以继续进行。(2)不可用浓盐酸代替稀盐酸,原因是浓盐酸易挥发出氯化氢气体,使制得的CO2不纯。(3)不可用碳酸钠或碳酸钙粉末代替石灰石(或大理石),这是由于碳酸钠或碳酸钙粉末与稀盐酸接触面积大,反应速率过快,不利于控制和收集二氧化碳气体。例题请你和小明一起进行实验室制取二氧化碳的探究。(一)选择药品小明对三组药品进行了研究,实验记录如下:组别药品实验现象①块状石灰石和稀盐酸产生气泡速率适中②块状石灰石和稀硫酸产生气泡速率缓慢并逐渐停止③粉末状石灰石和稀盐酸产生气泡速率很快对照实验①②在探究因素对制取二氧化碳气体产生的影响;对照实验①③在探究因素对制取二氧化碳气体产生的影响;小明选择第①组药品来制取二氧化碳,该组药品发生反应的化学方程式为;不选择第②组药品的原因是。(二)选择装置(1)写出图中带标号仪器的名称:①,②。(2)小明选择气体发生和收集的装置为(请在A~E中选择),验满方法是。(3)气体检验:将生成的气体通入石蕊溶液中,溶液变红,请...