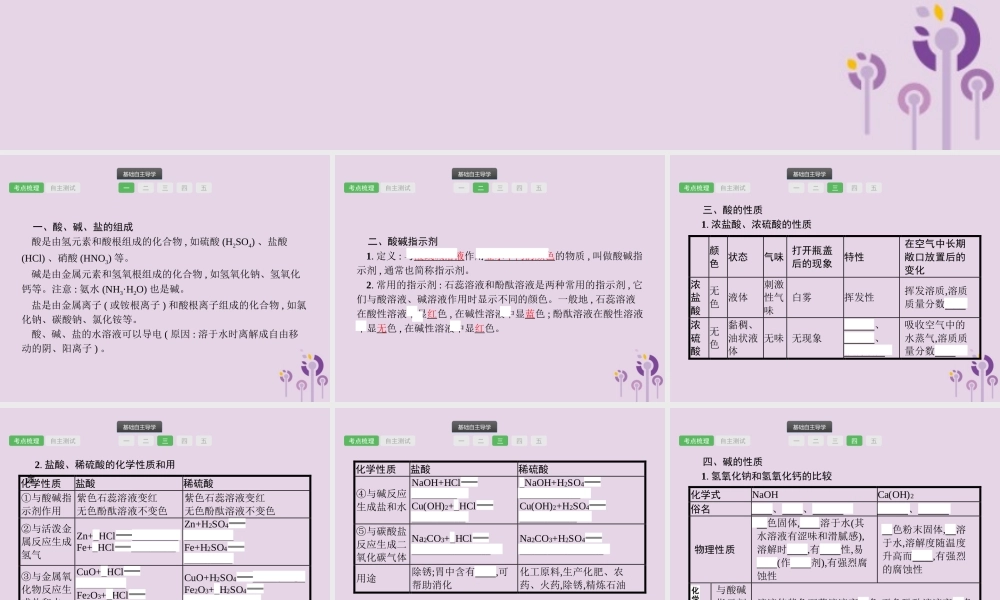
第十单元酸和碱基础自主导学基础自主导学考点梳理自主测试一二三四五一、酸、碱、盐的组成酸是由氢元素和酸根组成的化合物,如硫酸(H2SO4)、盐酸(HCl)、硝酸(HNO3)等。碱是由金属元素和氢氧根组成的化合物,如氢氧化钠、氢氧化钙等。注意:氨水(NH3·H2O)也是碱。盐是由金属离子(或铵根离子)和酸根离子组成的化合物,如氯化钠、碳酸钠、氯化铵等。酸、碱、盐的水溶液可以导电(原因:溶于水时离解成自由移动的阴、阳离子)。基础自主导学基础自主导学考点梳理自主测试一二三四五二、酸碱指示剂1.定义:与酸或碱溶液作用显示不同的颜色的物质,叫做酸碱指示剂,通常也简称指示剂。2.常用的指示剂:石蕊溶液和酚酞溶液是两种常用的指示剂,它们与酸溶液、碱溶液作用时显示不同的颜色。一般地,石蕊溶液在酸性溶液中显红色,在碱性溶液中显蓝色;酚酞溶液在酸性溶液中显无色,在碱性溶液中显红色。基础自主导学基础自主导学考点梳理自主测试一二三四五三、酸的性质1.浓盐酸、浓硫酸的性质颜色状态气味打开瓶盖后的现象特性在空气中长期敞口放置后的变化浓盐酸无色液体刺激性气味白雾挥发性挥发溶质,溶质质量分数变小浓硫酸无色黏稠、油状液体无味无现象吸水性、脱水性、强腐蚀性吸收空气中的水蒸气,溶质质量分数变小基础自主导学基础自主导学考点梳理自主测试一二三四五2.盐酸、稀硫酸的化学性质和用途化学性质盐酸稀硫酸①与酸碱指示剂作用紫色石蕊溶液变红无色酚酞溶液不变色紫色石蕊溶液变红无色酚酞溶液不变色②与活泼金属反应生成氢气Zn+2HClZnCl2+H2↑Fe+2HClFeCl2+H2↑Zn+H2SO4ZnSO4+H2↑Fe+H2SO4FeSO4+H2↑③与金属氧化物反应生成盐和水CuO+2HClCuCl2+H2OFe2O3+6HCl2FeCl3+3H2OCuO+H2SO4CuSO4+H2OFe2O3+3H2SO4Fe2(SO4)3+3H2O基础自主导学基础自主导学考点梳理自主测试一二三四五化学性质盐酸稀硫酸④与碱反应生成盐和水NaOH+HClNaCl+H2OCu(OH)2+2HClCuCl2+2H2O2NaOH+H2SO4Na2SO4+2H2OCu(OH)2+H2SO4CuSO4+2H2O⑤与碳酸盐反应生成二氧化碳气体Na2CO3+2HCl2NaCl+H2O+CO2↑Na2CO3+H2SO4Na2SO4+H2O+CO2↑用途除锈;胃中含有盐酸,可帮助消化化工原料,生产化肥、农药、火药,除锈,精炼石油注意浓硫酸、硝酸因具有很强的氧化性,与金属反应不生成氢气。基础自主导学基础自主导学考点梳理自主测试一二三四五四、碱的性质1.氢氧化钠和氢氧化钙的比较化学式NaOHCa(OH)2俗名火碱、烧碱、苛性钠熟石灰、消石灰物理性质白色固体,极易溶于水(其水溶液有涩味和滑腻感),溶解时放热,...