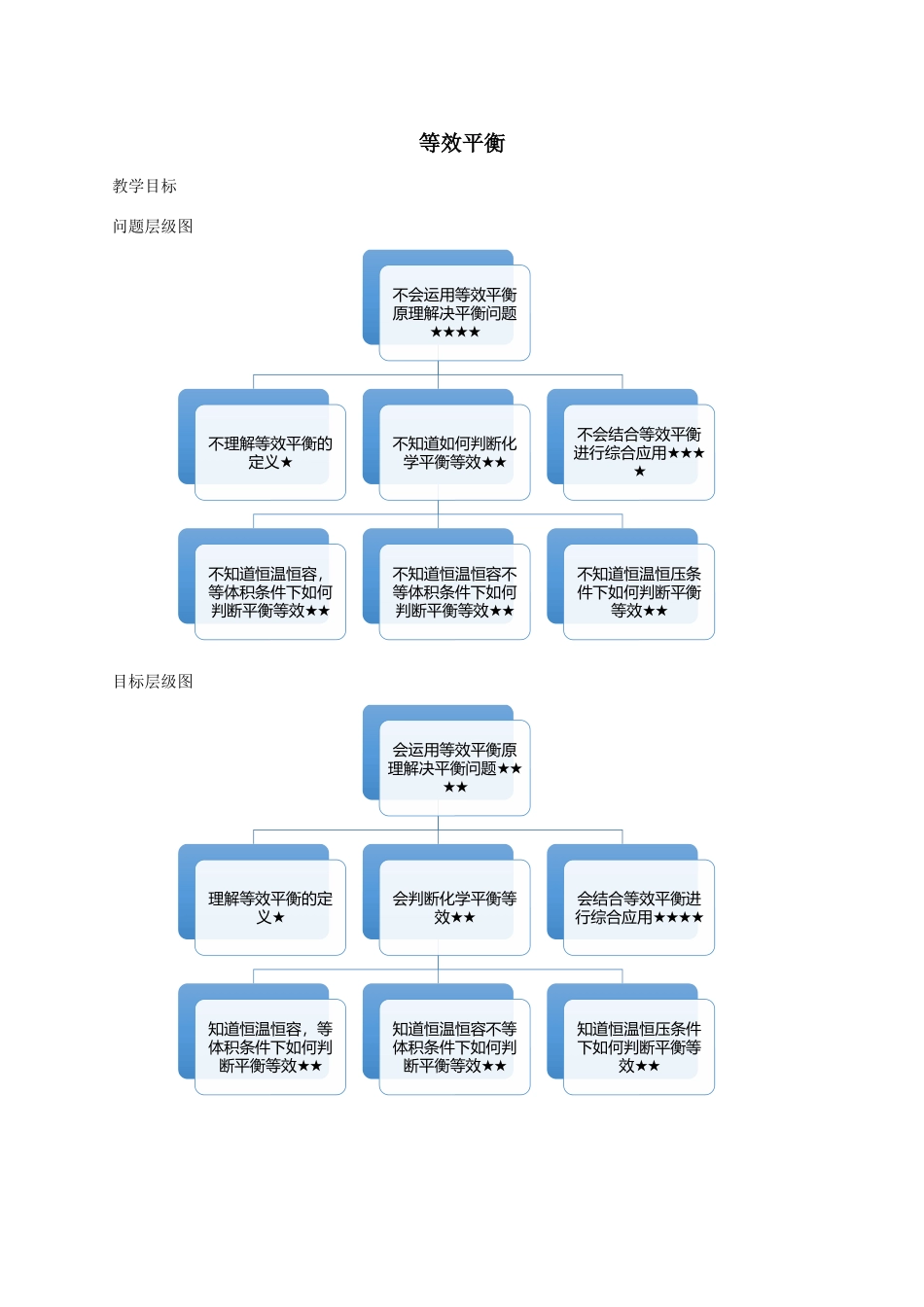
等效平衡教学目标问题层级图目标层级图不会运用等效平衡原理解决平衡问题★★★★不理解等效平衡的定义★不知道如何判断化学平衡等效★★不知道恒温恒容,等体积条件下如何判断平衡等效★★不知道恒温恒容不等体积条件下如何判断平衡等效★★不知道恒温恒压条件下如何判断平衡等效★★不会结合等效平衡进行综合应用★★★★会运用等效平衡原理解决平衡问题★★★★理解等效平衡的定义★会判断化学平衡等效★★知道恒温恒容,等体积条件下如何判断平衡等效★★知道恒温恒容不等体积条件下如何判断平衡等效★★知道恒温恒压条件下如何判断平衡等效★★会结合等效平衡进行综合应用★★★★一、理解等效平衡的定义(★)1、定义:在一定条件下(等温等容或等温等压),对同一可逆反应体系,起始时加入物质的物质的量不同,而达到化学平衡时,同种物质的百分含量相同。2、原理同一可逆反应,当外界条件一定时,反应无论从正反应开始,还是从逆反应开始,最后都能达到平衡状态。其中平衡混合物中各物质的含量相同。由于化学平衡状态与条件有关,而与建立平衡的途径无关。因而,同一可逆反应,从不同的状态开始,只要达到平衡时条件(温度、浓度、压强等)完全相同,则可形成等效平衡。[过关检测](3分钟)1、在等温等容条件下,可逆反应:2A(g)+B(g)3C(g)+D(s)起始物质的量如下表所示:序号ABCD①2mol1mol00②4mol2mol00③1mol0.5mol1.5mol0.5mol④01mol3mol1mol⑤003mol1mol上述反应达到平衡时,互为等效平衡的是哪几组?达到平衡后,哪些量相同?二、判断等效平衡的条件(★★)1、等温、等容条件下,对于左右气相物质的化学计量数不等的可逆反应,改变起始时加入物质的物质的量,若按可逆反应计量数之比换算成同一半边物质(一边倒),其物质的量对应相同,则它们互为等效平衡。2、等温、等容条件下,对于左右气相物质的化学计量数相等的可逆反应,改变起始时加入物质的物质的量,若按可逆反应计量数之比换算成同一半边物质(一边倒),其物质的量对应成比例,则它们互为等效平衡。3、等温、等压条件下,对于气体参加的反应,改变起始时加入物质的物质的量,若计量数之比换算成通一半边物质按可逆反应(一边倒)其物质的量对应成比例,则她们互为等效平衡[过关检测](10分钟)1、1.在等温等容条件下,可逆反应:2A(g)+B(g)3C(g)+D(g)ΔH=-Q1kJ·mol-1(Q1>0),起始物质的量如下表所示:序号ABCD①2mol1mol00②4mol2mol00③1mol0.5mol1.5mol...