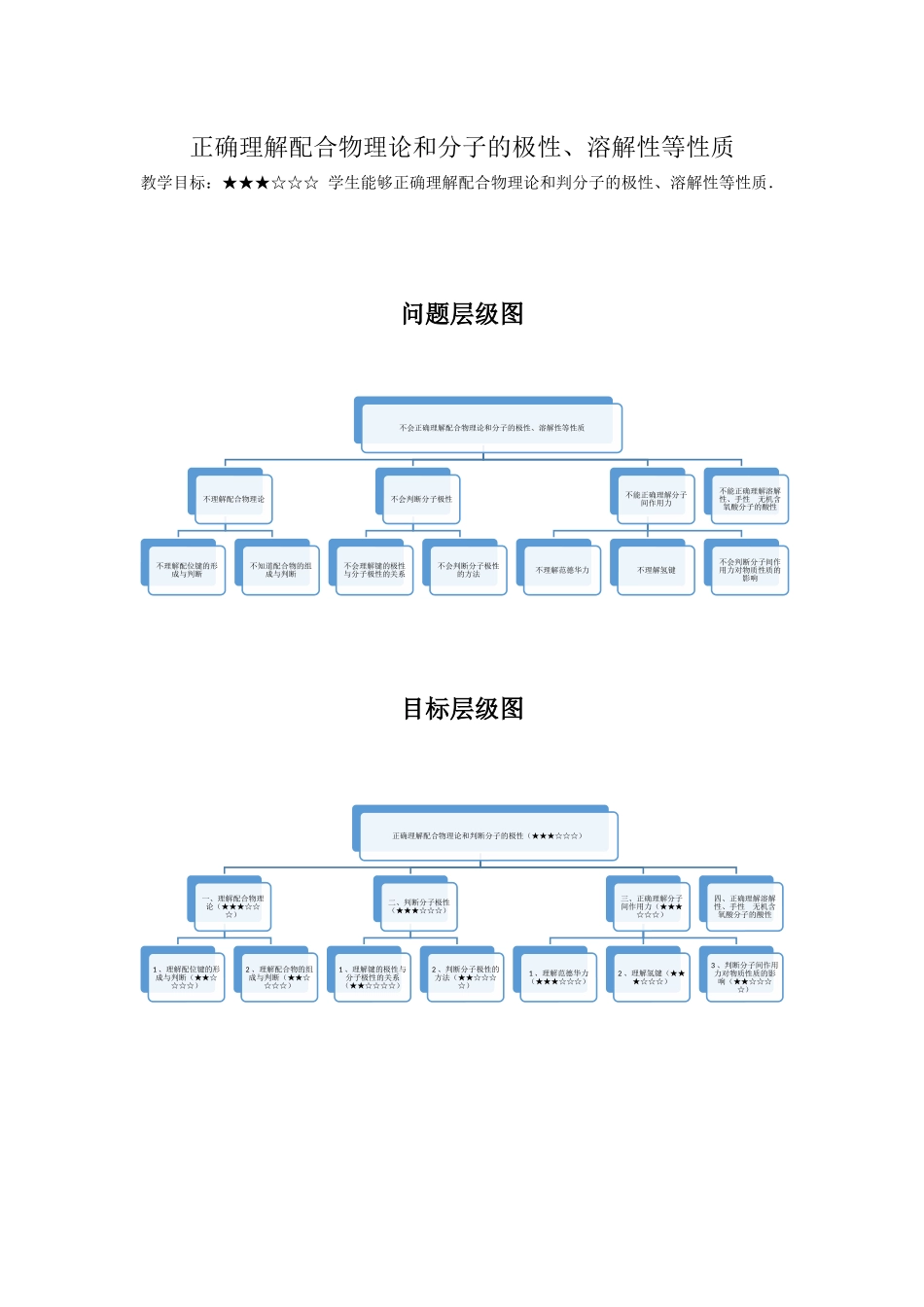
正确理解配合物理论和分子的极性、溶解性等性质教学目标:★★★☆☆☆学生能够正确理解配合物理论和判分子的极性、溶解性等性质.问题层级图目标层级图不会正确理解配合物理论和分子的极性、溶解性等性质不理解配合物理论不理解配位键的形成与判断不知道配合物的组成与判断不会判断分子极性不会理解键的极性与分子极性的关系不会判断分子极性的方法不能正确理解分子间作用力不理解范德华力不理解氢键不会判断分子间作用力对物质性质的影响不能正确理解溶解性、手性无机含氧酸分子的酸性正确理解配合物理论和判断分子的极性(★★★☆☆☆)一、理解配合物理论(★★★☆☆☆)1、理解配位键的形成与判断(★★☆☆☆☆)2、理解配合物的组成与判断(★★☆☆☆☆)二、判断分子极性(★★★☆☆☆)1、理解键的极性与分子极性的关系(★★☆☆☆☆)2、判断分子极性的方法(★★☆☆☆☆)三、正确理解分子间作用力(★★★☆☆☆)1、理解范德华力(★★★☆☆☆)2、理解氢键(★★★☆☆☆)3、判断分子间作用力对物质性质的影响(★★☆☆☆☆)四、正确理解溶解性、手性无机含氧酸分子的酸性正确理解配合物理论和分子的极性、溶解性等性质一、理解配合物理论(★★★☆☆☆)(1)理解配位键的形成与判断(★★☆☆☆☆)1.配位键:配位键是一种特殊的。只是当中共用电子对是由其中一原子供应,另一原子提供轨道。2.配位键的形成条件是(1)一方,(2)一方。【过关检测】(3min)1.下列微粒中含配位键的是()①N2H②CH4③OH-④NH⑤Fe(CO)3⑥Fe(SCN)3⑦H3O+⑧[Ag(NH3)2]OHA.①②④⑦⑧B.③④⑤⑥⑦C.①④⑤⑥⑦⑧D.全部(2)理解配合物的组成与判断(★★☆☆☆☆)1.配位化合物:通常把金属离子(或原子)与某些分子或离子(称为配体)以结合形成的化合物称为配位化合物。2.配位化合物由、、三部分组成。【过关检测】(1min)1.下列化合物中属于配合物的是()①CuSO4·5H2O②K2PtCl6③KCl·CuCl2④Cu(NH2CH2COO)2⑤KCl·MgCl2·6H2O⑥Cu(CH3COO)2A.①③④⑥B.②③⑤C.①②D.①③⑤二、判断分子极性(★★★☆☆☆)(1)理解键的极性与分子极性的关系(★★☆☆☆☆)1.键的极性极性键:由原子形成的共价键,电子对偏移,两个键合原子,一个呈,另一个呈。非极性键:由原子形成的共价键,电子对偏移。2.分子的极性极性分子:分子中正电中心和负电中心,使分子的一部分呈正电性,另一部分呈负电性,即键的极性的向量和零。如HCl、H2O、NH3、H...