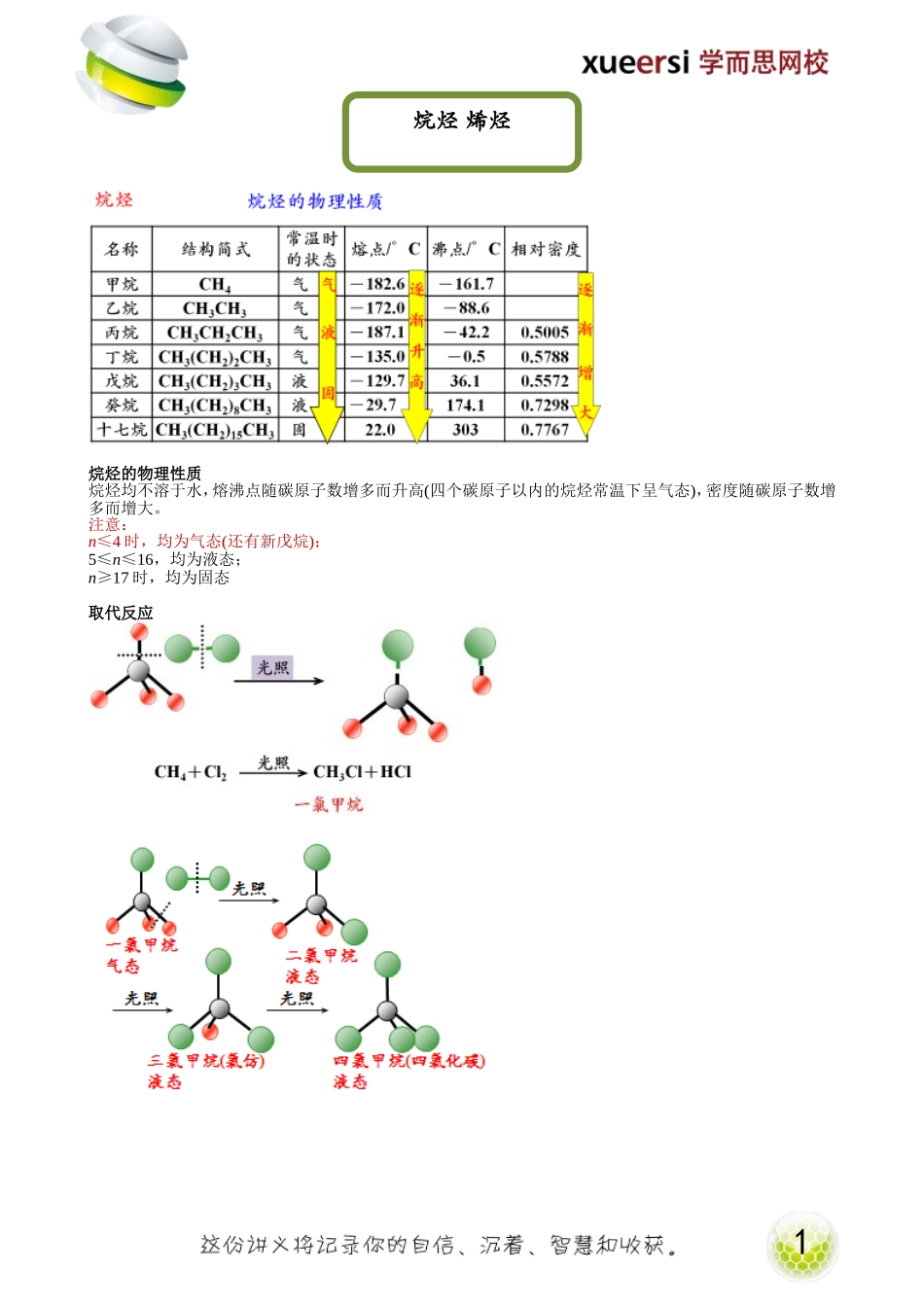
1烷烃的物理性质烷烃均不溶于水,熔沸点随碳原子数增多而升高(四个碳原子以内的烷烃常温下呈气态),密度随碳原子数增多而增大。注意:n≤4时,均为气态(还有新戊烷);5≤n≤16,均为液态;n≥17时,均为固态取代反应烷烃烯烃2【例1】已知某种有机物的化学式为C4H4,分子如图所示,若将该有机物与适量氯气混合后光照,则生成氯代产物的种类最多有()A.2种B.4种C.5种D.6种【例2】1mol乙烷在光照条件下,最多可以与()molCl2发生取代反应A.4molB.8molC.2molD.6mol烷烃的热裂化反应【例3】C8H18经多步裂化(指在隔绝空气条件下高温加热),最后完全转化为C4H8、C3H6、C2H4、C2H6、CH4五种气体的混合物。该混合物的平均相对分子质量可能是()A.28B.30C.38D.40烷烃的同分异构体1.书写规则:2.几种重要的烷烃及烷基:3【例4】化学式为C7H16的烷烃分子中,含有三个甲基的同分异构体的数目有()A.2种B.3种C.4种D.5种【例5】烯烃的顺反异构CH3CH=CHCH342-丁烯思考:2-丁烯中与碳碳双键相连的两个碳原子、两个氢原子是否处于同一平面?如处于同一平面,与碳碳双键相连的两个碳原子是处于双键的同侧还是异侧?如果每个双键碳原子连接了两个不同的原子或原子团,双键上的4个原子或原子团在空间就有两种不同的排列方式,产生两种不同的异构,即顺反异构。形成顺反异构的条件:1.具有碳碳双键2.组成双键的每个碳原子必须连接两个不同的原子、原子团。(若双键的任何一个碳原子所连接的两个原子或原子团相同时就没有顺反异构现象)烯烃的化学性质1.氧化反应乙烯在空气中燃烧生成二氧化碳和水。乙烯含碳量高,碳没有得到充分燃烧,所以有黑烟产生。52.加成反应有机物分子中双键(或三键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应。此反应可定性鉴定C=C的存在乙烯还可与水、氢气、卤化氢、氯气等在一定条件下发生加成反应3.加成聚合反应【例6】某含有1个碳碳双键的烯烃,氢化后产物的结构式如下图,则此烯烃可能的结构有()A.6种B.7种C.8种D.9种6【例7】某气态烷烃20mL,完全燃烧时,正好消耗同温同压下的氧气100mL,该烃的化学式是()A.C2H6B.C3H8C.C4H10D.C5H12【例8】某种烷烃11g完全燃烧时,需要标况下28L氧气,该烷烃()A.C5H12B.C4H10C.C3H8D.C2H6【例9】两种气态烃以任意比例混合,在105℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍为10L。下列各组分混合烃中,符合此条件是()A.CH4,C2H4B.CH4,C3H6C.C2H4,C3H4D.C2H2,C3H6