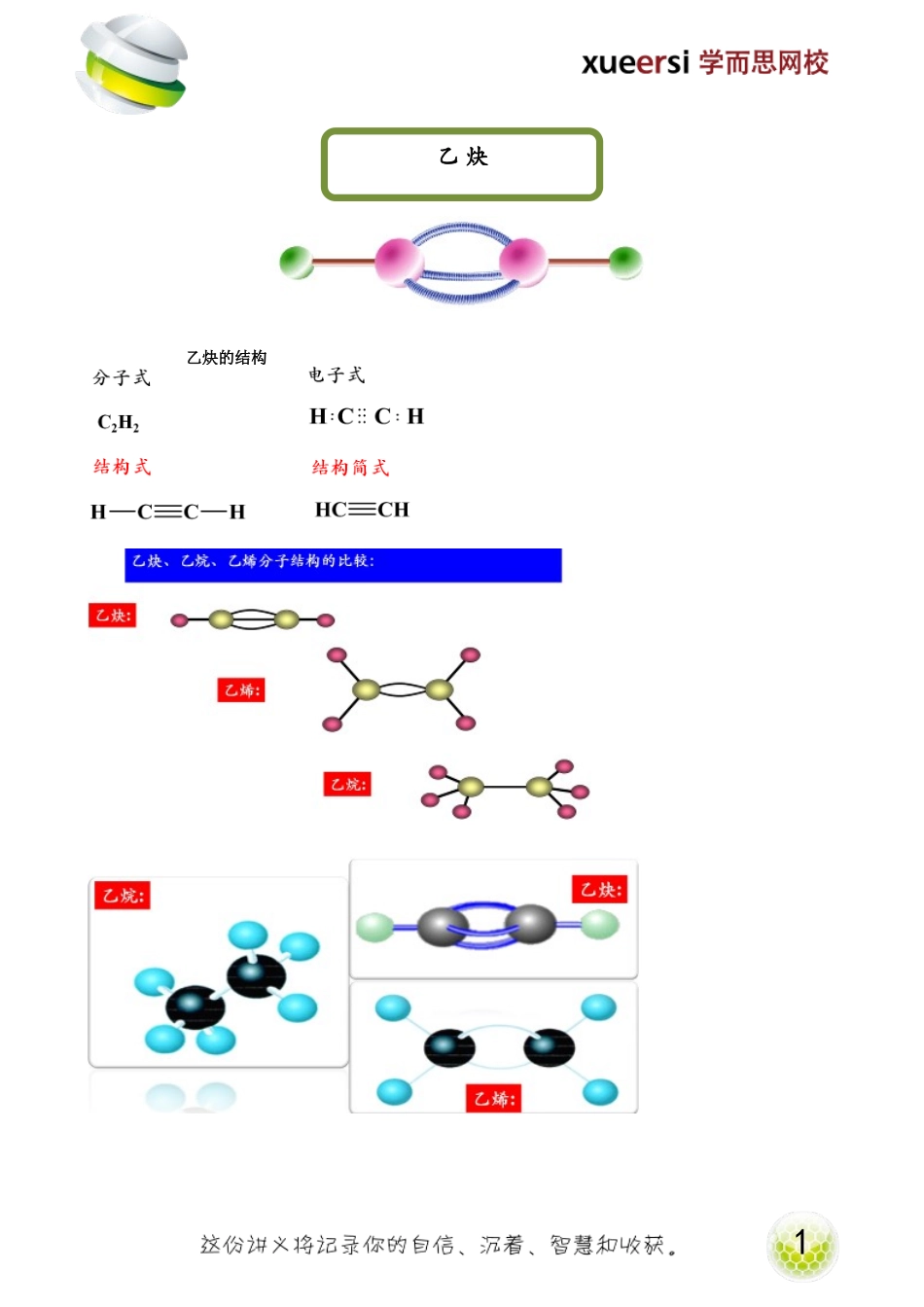
1乙炔的结构乙炔2【例1】CH3-CH=CH-C≡C-CF3分子结构的下列叙述中,正确的是()A.6个碳原子有可能都在一条直线上B.6个碳原子不可能在一条直线上C.6个碳原子有可能都在同一平面上D.6个碳原子不可能都在同一平面上乙炔的物理性质纯的乙炔是没有颜色、没有臭味的气体。密度是1.16克/升,比空气稍轻。微溶于水,易溶于有机溶剂。【例2】CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属离子型碳化物,请通过对CaC2制C2H2的反应进行思考,从中得到必要的启示,写出下列反应的产物:A.ZnC2水解生成()B.Al4C3水解生成()C.Mg2C3水解生成()D.Li2C2水解生成()3.装置:3不用启普发生器制取乙炔的原因1.因为碳化钙与水反应剧烈,启普发生器不易控制反应;2.反应放出大量热,启普发生器是厚玻璃壁仪器,容易因胀缩不均,引起破碎;3.生成物Ca(OH)2微溶于水,易形成糊状泡沫堵塞导气管和球形漏斗的下口;4.关闭导气阀后,水蒸气仍与电石作用,不能达到“关之即停”的目的。能不能用制取氢气时所采用的那种简易装置?为什么?实验室中使用分液漏斗而不使用长颈漏斗,因为长颈漏斗不能控制水的用量。水加太多,反应会太剧烈。下列那种装置可以用来做为乙炔的收集装置?4.收集5.净化因为电石中含有CaS、Ca3P2等,也会与水反应,产生H2S、PH3等气体,所以用电石制得的乙炔气体有难闻的臭味。4实验中采用块状CaC2和饱和食盐水,为什么?实验中为什么要采用分液漏斗?制出的乙炔气体为什么先通入硫酸铜溶液?还可以用什么试剂来清除杂质?探究一实验室若需制备较多量的乙炔,如何从装置上改进?探究二1.若要控制乙炔产生的速率,如何从装置上改进?2.若要控制乙炔产生的速率,如何从试剂上改进?探究三1.实验室制得的乙炔并非没有气味而是有特殊难闻臭味的气体,这种气体是什么?纯净的乙炔没有气味,但由电石产生的乙炔常因混有H2S等杂质而有特殊难闻的臭味。2.H2S对本实验有影响吗?为什么?H2S具有较强还原性,易被酸性高锰酸钾溶液氧化,使其褪色,因而会对该实验造成干扰。53.如何避免H2S造成的干扰,验证乙炔能使酸性高锰酸钾溶液褪色?请选择必要的装置(可重复使用)。4.如何从试剂上进行改进,避免H2S造成的干扰,验证乙炔能使酸性高锰酸钾溶液褪色?探究四1.该实验进行一段时间后,饱和食盐水滴下速度显著减小,试分析原因。2.如何改进装置,解决这个问题?6【例3】⑴为控制水与电石的反应速率,并得到平稳气流采取的措施是____...