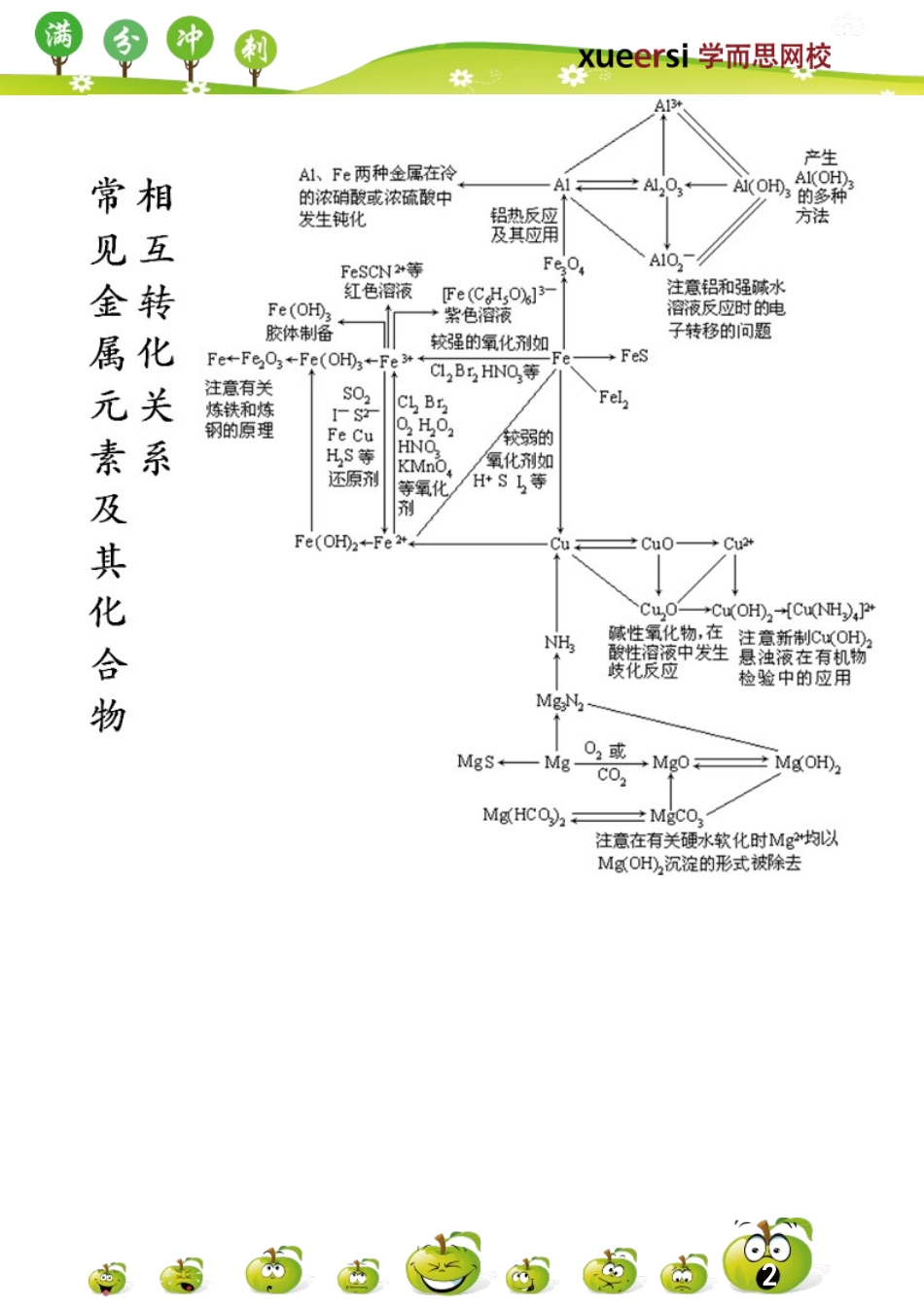
1元素化合物知识体系:结合元素周期律,总结和拓展元素知识23451.原子半径⑴除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小;⑵同一族的元素从上到下,随电子层数增多,原子半径增大。2.元素化合价⑴除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外);⑵同一主族的元素的最高正价、负价均相同3.单质的熔点⑴同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减;⑵同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增4.元素的金属性与非金属性⑴同一周期的元素从左到右金属性递减,非金属性递增;⑵同一主族元素从上到下金属性递增,非金属性递减。5.最高价氧化物和水化物的酸碱性元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价氧化物的水化物的酸性越强。6.非金属气态氢化物元素非金属性越强,气态氢化物越稳定。同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;同主族非金属元素的非金属性越强,其气态氢化物水溶液的酸性越弱。7.单质的氧化性、还原性一般元素的金属性越强,其单质的还原性越强,其氧化物的氧离子氧化性越弱;元素的非金属性越强,其单质的氧化性越强,其简单阴离子的还原性越弱。【例1】已知Cs在元素周期表的位置:第六周期,第IA族,推测其原子结构及化学性质。【例2】已知某元素原子有六个电子层,最外层2个电子,试推测其在周期表的位置及化学性质【例3】溴化碘(IBr)的化学性质与卤素单质相似,能与大多数金属反应生成卤化物,与水反应的化学方程式是IBr+H2O=HBr+HIO,下列关于IBr的叙述错误的是()A.固体IBr是由分子构成的B.与NaOH反应生成NaBr和NaIOC.与水反应既是氧化剂又是还原剂D.在很多反应中是氧化剂6【例4】X、Y、Z为三个不同短周期非金属元素的单质,在一定条件下有如下反应:Y+X→A(气),Y+Z→B(气)。请针对以下两种情况回答:⑴若常温下X、Y、Z均为气体,且A和B化合生成固体C时有白烟产生,则:①Y的化学式是;②生成固体C的化学方程式是。⑵若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:①B的化学式是。②向苛性钠溶液中通入过量的A,所发生反应的离子方程式是;③将Y与⑴中某单质的水溶液充分反应可生成两种强酸,该反应的化学方程式是。【例5】已知甲、乙...