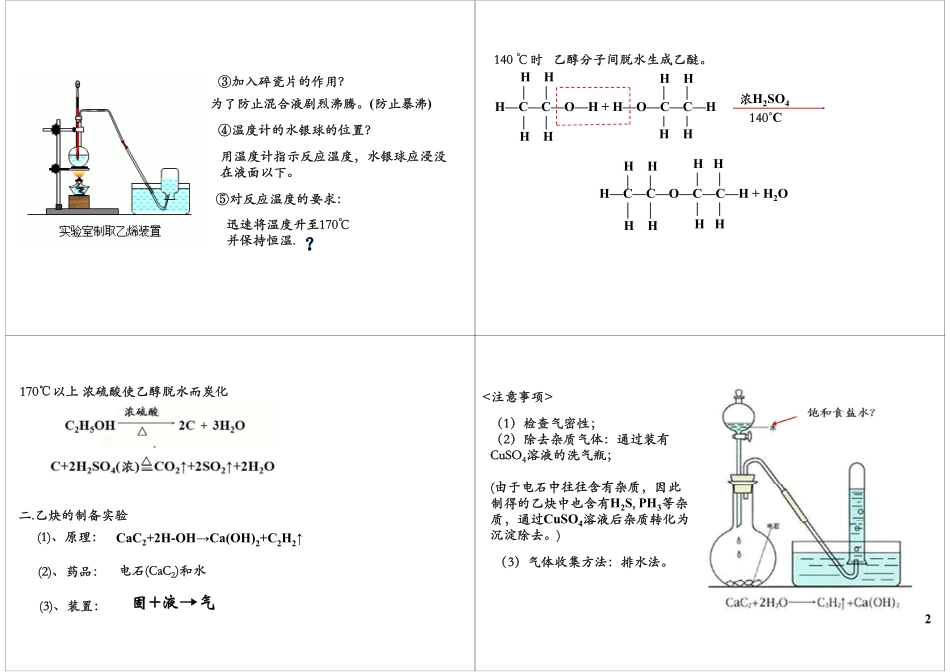
有机化学实验(一)主讲老师:江成答疑邮箱:huaxuebaidujiang@163.com课程导航:课程导航基础知识点讲解1•乙烯的制备实验12•乙炔的制备实验23•乙酸乙酯的制备实验31乙烯的工业制法一.乙烯的制备实验1.乙烯的工业制法乙烯是一种重要的基本化工原料,其产量可以用来衡量一个国家的石油化工发展水平目前工业上获得乙烯的主要途径是石油的裂的石油化工发展水平。目前,工业上获得乙烯的主要途径是石油的裂解法,再经过净化和分离,就可以得到所需纯度的乙烯。2.乙烯的实验室制法实验室常用加热酒精和浓硫酸的混合物,制取乙烯(CH2=CH2)(1)反应原理:(2)实验装置(2)实验装置:液+液→气液液气3.注意事项:①浓硫酸与酒精的如何混合?混合时应将浓硫酸缓缓加入酒精中并不断搅拌。酒精中并断拌②浓硫酸在反应中起的作用?催化剂、脱水剂。1③加碎瓷片的作③加入碎瓷片的作用?为了防止混合液剧烈沸腾。(防止暴沸)④温度计的水银球的位置?用温度计指示反应温度,水银球应浸没在液面以下。⑤对反应温度的要求:迅速将温度升至170℃迅速将温度升至170℃并保持恒温.HHHH140℃时乙醇分子间脱水生成乙醚。HHH—C—C—O—H+H—O—C—C—HHH浓H2SO4˚CHHHH140˚CHHHHH—C—C—O—C—C—H+H2OHHHHHHHH170℃以上浓硫酸使乙醇脱水而炭化二.乙炔的制备实验CaC2+2H-OH→Ca(OH)2+C2H2↑(1)、原理:电石(CaC2)和水液气(2)、药品:固+液→气(3)、装置:<注意事项>(1)检查气密性;(2)除去杂质气体:通过装有CuSO4溶液的洗气瓶;(由于电石中往往含有杂质因此(由于电石中往往含有杂质,因此制得的乙炔中也含有H2S,PH3等杂质,通过CuSO4溶液后杂质转化为质,通过CuSO4溶液后杂质转化为沉淀除去。)(3)气体收集方法排水法(3)气体收集方法:排水法。2(1)原理:三.乙酸乙酯的制备实验(1)原理:CH3COOH+HOCH2CH3浓硫酸△+H2OCH3COOCH2CH3△(2)反应条件:反应物、生成物的状态:沸点常温下状态乙醇785℃液体乙醇78.5℃液体乙酸117.9℃液体乙酸乙酯7706℃液体乙酸乙酯77.06℃液体制备乙酸乙酯的简易装置图反应特点:特①通常反应速率较小;②反应是可逆的,乙酸乙酯的产率低。Na2CO3乙酸乙酯制取注意事项1.装药品的顺序如何?先加乙醇再加浓硫酸最后加乙酸先加乙醇,再加浓硫酸,最后加乙酸。2.浓硫酸的作用是什么?催化剂,吸水剂。3加碎瓷片的作用是什么?3.加碎瓷片的作用是什么?防止液体剧烈沸腾,暴沸4.杂质:乙酸;乙醇(均易挥发)5.饱和Na2CO3溶液...