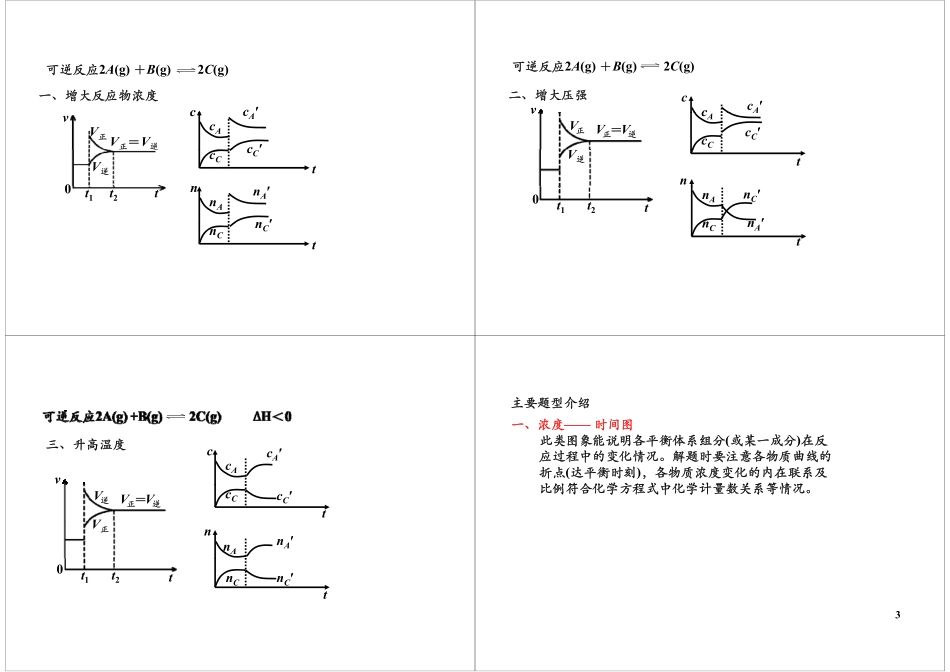
化学平衡综合(三)化学平衡与图像思考:根据下列图示,分别改变的是什么条件——化学平衡与图像vv00t0t1t2t0t1t2vvt0t1t2t0t1t21.浓度:可逆反应2A(g)+B(g)2C(g)vvV正=V逆V正V正00正逆V正=V逆V逆正V逆增大反应物浓度降低生成物浓度t0t1t2t0t1t2vvV正=V逆V正=V逆V逆V逆增大生成t0t1t2t0t1t2V正V正降低反应物浓度增大生成物浓度tt1t2tt1t22.温度:vvV正=V逆V逆vV正V正=V逆V正V逆t0t1t2t0t1t2升高温度降低温度3.压强:可逆反应2A(g)+B(g)2C(g)vvvvV正=V逆V正V逆V正=V逆V逆t0t1t2t0t1t2V正增大压强减小压强1可逆反应2A(g)+B(s)2C(g)+Q可逆反应2A(g)+B(s)2C(g)+QvvV正=V逆V正V正=V逆V正V′正=V′逆t0t1t0t1V逆V逆t1t1增大压强减小压强vvvV′=V′vV正=V逆V正V′正=V′逆t0tV逆tt1催化剂:只同等程度的影响正逆反应速的影响正、逆反应速率,不改变化学平衡c-t图像cA′ccA′cccAcC′cAcCAcC′BcAcC降低温度增大压强CtA.cCcctB.降低CcAccA′′cAcCcA′c′减小压强降低的浓度tC.cCcC′tD.cCcC′n-t图像nA′nnAnc′AnAnCnAnn′nC′升高温度增大压强tA.CtB.nCnAnnAnA′nnAnA′减小压强减少C的物质的量tC.nCnC′tD.nCnC′减小压强2可逆反应2A(g)+B(g)2C(g)(g)(g)(g)一、增大反应物浓度cc′ccAc′cAvV正=V逆V正tcCcCn′0V逆nnAnA′n′t0t1t2tnCnC可逆反应2A(g)+B(g)2C(g)二、增大压强cccA′vcAcCcC′vV正=V逆V正tnV逆nAnn′nC′t0t1t2tnCnA三、升高温度v三、升高温度ccAcA′V正=V逆VV逆tcCcC′V正nnA′nAt0t1t2tnC′nCt主要题型介绍一、浓度——时间图此类图象能说明各平衡体系组分(或某一成分)在反应过程中的变化情况。解题时要注意各物质曲线的折点(达平衡时刻),各物质浓度变化的内在联系及比例符合化学方程式中化学计量数关系等情况比例符合化学方程式中化学计量数关系等情况。3⑴写出化学反应方程式:【例1】cCA⑵求反应物的转化率:32B10tc⑴写出化学反应方程式:【例2】Bc⑴写出化学反应方程式:⑵求反应物的转化率:例43ACt210t0二速率时间图二、速率——时间图此类图象定性地揭示了v正、v逆随时间(含条件改变对速率的影响)而变化的规律体现了平衡的变对速率的影响)而变化的规律,体现了平衡的“动、等、定、变”的基本特征,以及平衡移动的方向。可用于:⑴(已知反应)判断引起平衡移动的因素⑴(已知反应)判断引起平衡移动的因素。⑵已知引起平衡移动的因素,判断反应是吸热或放热,反应前后气体体积的变化。...