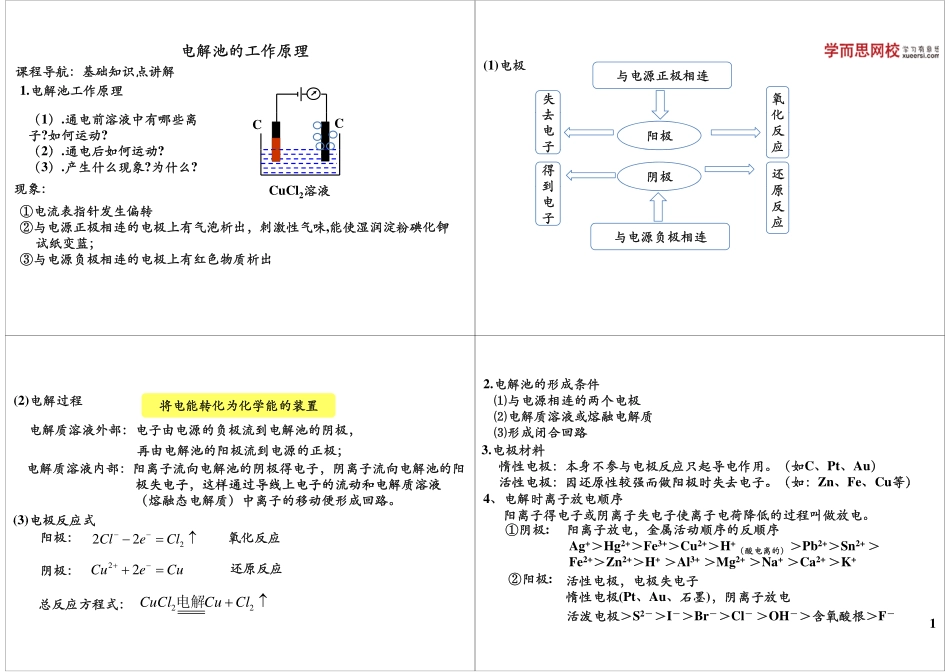
课程导航:基础知识点讲解电解池的工作原理课程导航基础知识点讲解1.电解池工作原理CC(1).通电前溶液中有哪些离子?如何运动?(2)通电后如何运动?(2).通电后如何运动?(3).产生什么现象?为什么?CCl溶液现象CuCl2溶液①电流表指针发生偏转②与电源正极相连的电极上有气泡析出刺激性气味能使湿润淀粉碘化钾现象:②与电源正极相连的电极上有气泡析出,刺激性气味,能使湿润淀粉碘化钾试纸变蓝;③与电源负极相连的电极上有红色物质析出③与电源负极相连的电极上有红色物质析出(1)电极与电源正极相连与电源正极相连失去氧化阳极去电子化反应子应阴极得到还原到电子原反应与电源负极相连子应(2)电解过程将电能转化为化学能的装置电解质溶液外部:电子由电源的负极流到电解池的阴极,将转学装再由电解池的阳极流到电源的正极再由电解池的阳极流到电源的正极;电解质溶液内部:阳离子流向电解池的阴极得电子,阴离子流向电解池的阳极失电子这样通过导线上电子的流动和电解质溶液极失电子,这样通过导线上电子的流动和电解质溶液(熔融态电解质)中离子的移动便形成回路。(3)电极反应式(3)电极反应式阳极:222CleCl氧化反应阴极:22CueCu电解还原反应总反应方程式:22CuClCuCl电解2.电解池的形成条件⑴与电源相连的两个电极⑵电解质溶液或熔电解质⑵电解质溶液或熔融电解质⑶形成闭合回路3电极材料3.电极材料惰性电极:本身不参与电极反应只起导电作用。(如C、Pt、Au)活性电极:因还原性较强而做阳极时失去电子。(如:Zn、Fe、Cu等)活性电极:因还原性较强而做阳极时失去电子。(如:Zn、Fe、Cu等)4、电解时离子放电顺序阳离子得电子或阴离子失电子使离子电荷降低的过程叫做放电。①阴极:阳离子放电,金属活动顺序的反顺序Ag+>Hg2+>Fe3+>Cu2+>H+(酸电离的)>Pb2+>Sn2+>F2+>Z2+>H+>Al3+>M2+>N+>C2+>K+Fe2+>Zn2+>H+>Al3+>Mg2+>Na+>Ca2+>K+②阳极:活性电极,电极失电子惰性电极(PtAu石墨)阴离子放电惰性电极(Pt、Au、石墨),阴离子放电活泼电极>S2->I->Br->Cl->OH->含氧酸根>F-15.电解类型I区II区电解类型I区II区Ag+Hg2+Fe3+Cu2+H+Pb2+…Al3+…K+S2-I-Br-Cl-OH-含氧酸根F-SIBrClOH含氧酸根FIII区Ⅳ区I区与III区:电解电解质型与Ⅳ放生酸型I区与Ⅳ区:放O2生酸型II区与III区:放H2生碱型II区与Ⅳ区:电解水型II区与Ⅳ区:电解水型I区与III区:电解电解质型实例电极反应式电解方程...