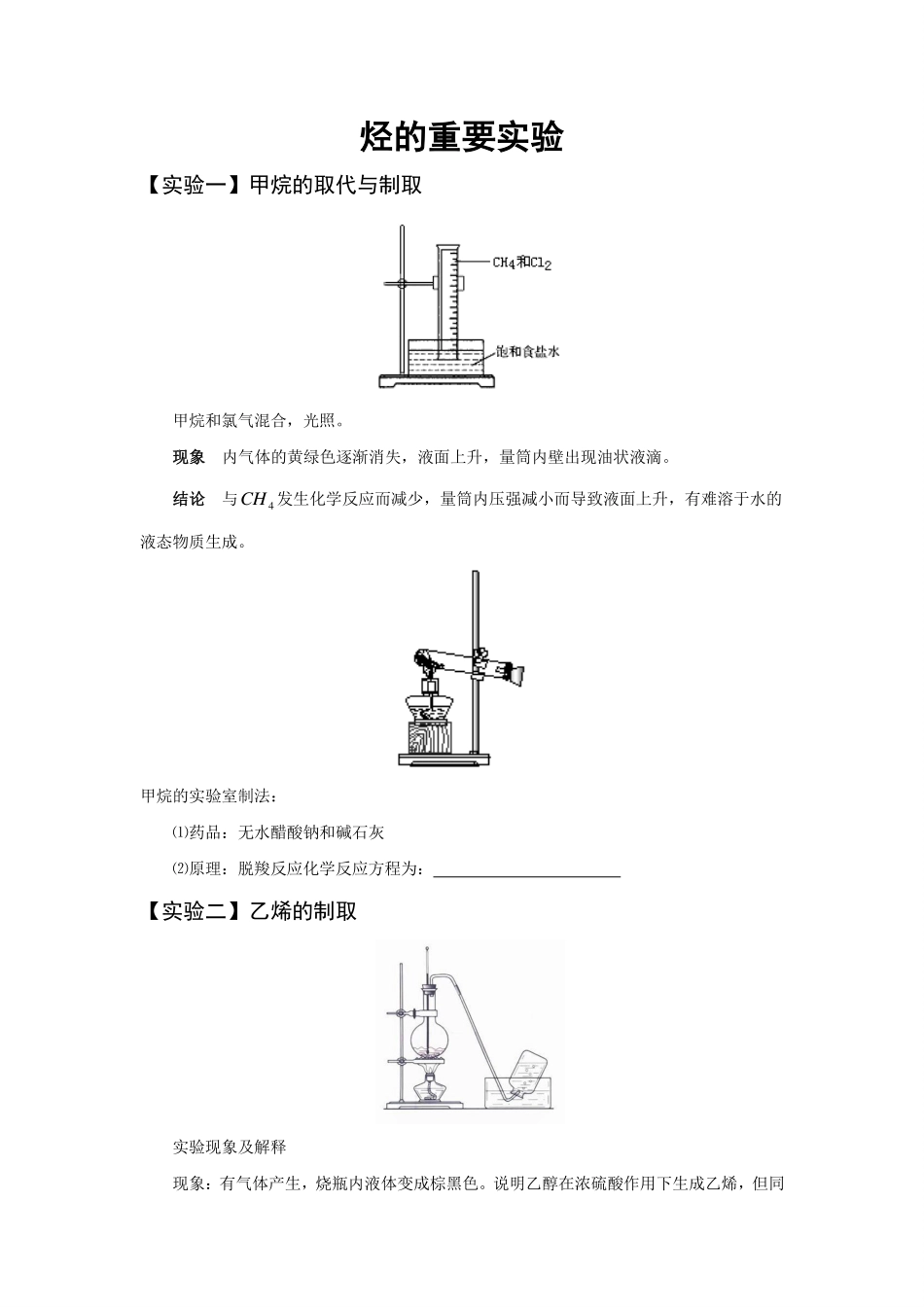
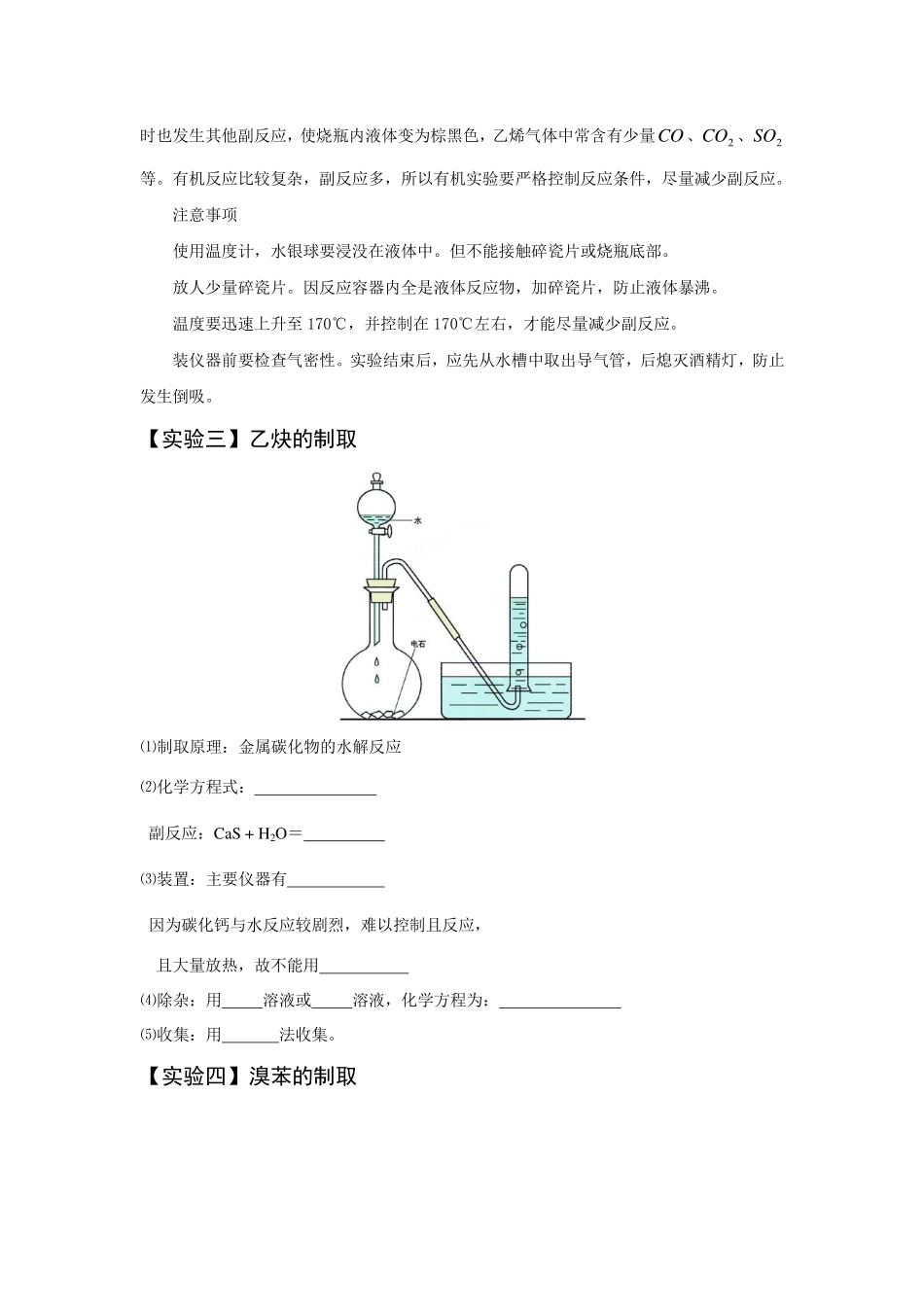
烃的重要实验【实验一】甲烷的取代与制取甲烷和氯气混合,光照。现象内气体的黄绿色逐渐消失,液面上升,量筒内壁出现油状液滴。结论与4CH发生化学反应而减少,量筒内压强减小而导致液面上升,有难溶于水的液态物质生成。甲烷的实验室制法:⑴药品:无水醋酸钠和碱石灰⑵原理:脱羧反应化学反应方程为:【实验二】乙烯的制取实验现象及解释现象:有气体产生,烧瓶内液体变成棕黑色。说明乙醇在浓硫酸作用下生成乙烯,但同时也发生其他副反应,使烧瓶内液体变为棕黑色,乙烯气体中常含有少量CO、2CO、2SO等。有机反应比较复杂,副反应多,所以有机实验要严格控制反应条件,尽量减少副反应。注意事项使用温度计,水银球要浸没在液体中。但不能接触碎瓷片或烧瓶底部。放人少量碎瓷片。因反应容器内全是液体反应物,加碎瓷片,防止液体暴沸。温度要迅速上升至170℃,并控制在170℃左右,才能尽量减少副反应。装仪器前要检查气密性。实验结束后,应先从水槽中取出导气管,后熄灭酒精灯,防止发生倒吸。【实验三】乙炔的制取⑴制取原理:金属碳化物的水解反应⑵化学方程式:副反应:CaS+H2O=⑶装置:主要仪器有因为碳化钙与水反应较剧烈,难以控制且反应,且大量放热,故不能用⑷除杂:用溶液或溶液,化学方程为:⑸收集:用法收集。【实验四】溴苯的制取反应物苯和液溴(不能用溴水)反应条件催化剂反应装置如图圆底烧瓶上的导管起导气和冷凝作用。实验操作检查气密性后,把苯和少量纯溴放在烧瓶里,加入少量铁屑(催化剂)。反应完毕后,向锥形瓶中滴加3AgNO溶液,将烧瓶里的液体倒人盛冷水的烧杯。实验现象导管口附近出现白雾,锥形瓶内有浅黄色沉淀,烧杯底部有褐色不溶于水的液体。实验结论苯与液溴反应生成HBr和溴苯(纯溴苯为无色液体,因溶有溴而显褐色,可用NaOH溶液和分液的方法除去溴杂质)。【实验五】苯的硝化反应反应物苯和浓硝酸反应条件:催化剂浓硫酸的温度在55℃~60℃。反应装置采用水浴加热(受热均匀,易控制温度),大试管上长导管起连通大气和冷凝的作用。实验操作先加浓硝酸,再加浓硫酸,摇匀冷却到60℃以下,最后加入苯,反应完毕后,将试管内液体倒人盛有冷水的另一支试管中。实验现象苯逐渐减少,盛有冷水的另一支试管的底部有不溶于水的油状物。实验结论苯与浓硝酸发生反应,生成不溶于水密度比水大的硝基苯。此反应叫硝化反应。