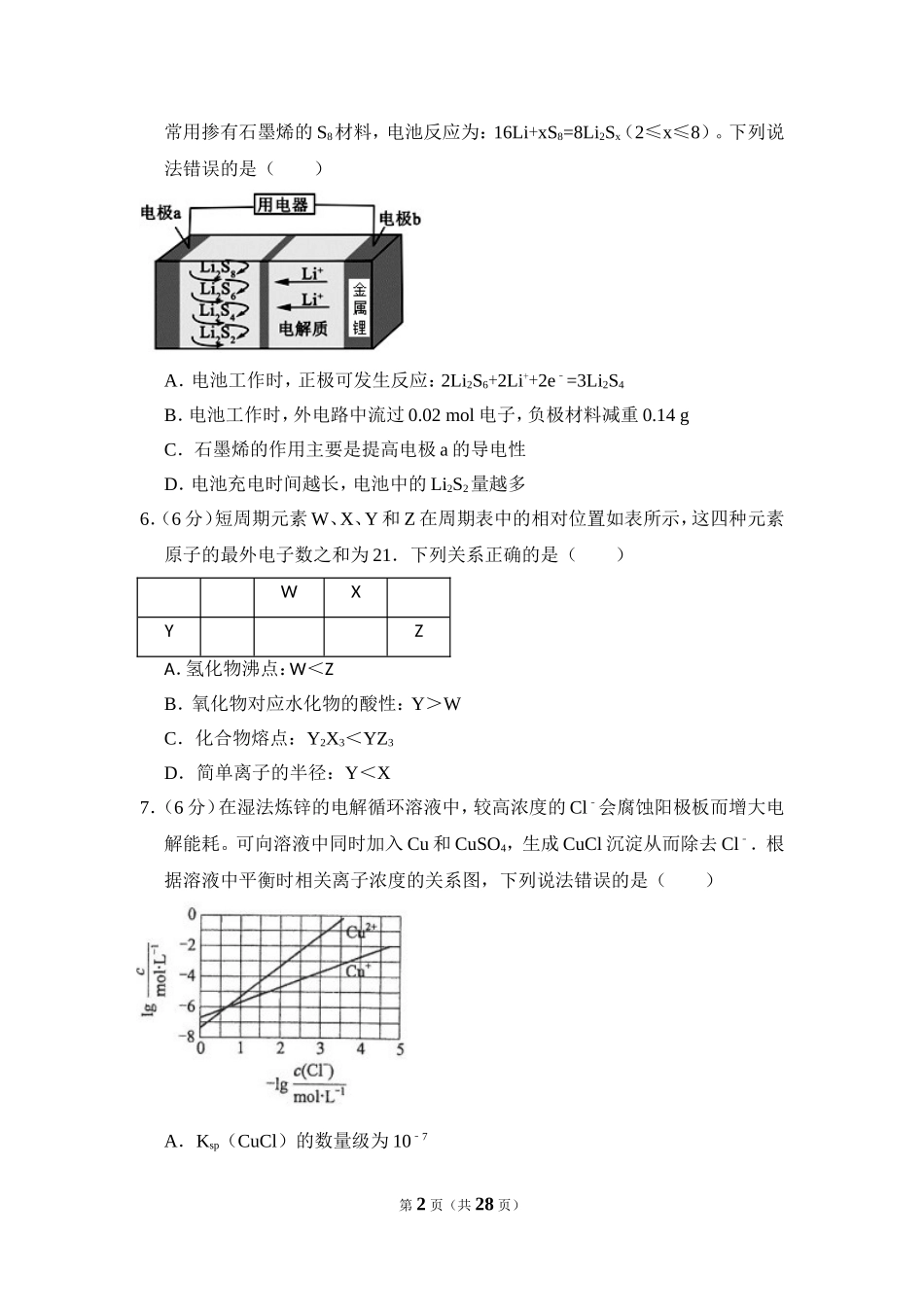
2017年全国统一高考化学试卷(新课标Ⅲ)一、选择题:本题共7个小题,每小题6分,共42分.在每小题给出的四个选项中只有一项是符合题目要求的.1.(6分)化学与生活密切相关。下列说法错误的是()A.PM2.5是指粒径不大于2.5μm的可吸入悬浮颗粒物B.绿色化学要求从源头上消除或减少生产活动对环境的污染C.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放D.天然气和液化石油气是我国目前推广使用的清洁燃料2.(6分)下列说法正确的是()A.植物油氢化过程中发生了加成反应B.淀粉和纤维素互为同分异构体C.环己烷与苯可用酸性KMnO4溶液鉴别D.水可以用来分离溴苯和苯的混合物3.(6分)下列实验操作规范且能达到目的是()目的操作A.取20.00mL盐酸在50mL酸式滴定管中装入盐酸,调整初始读数为30.00mL后,将剩余盐酸放入锥形瓶B.清洗碘升华实验所用试管先用酒精清洗,再用水清洗C.测定醋酸钠溶液pH用玻璃棒蘸取溶液,点在湿润的pH试纸上D.配制浓度为0.010mol/L的KMnO4溶液称取KMnO4固体0.158g,放入100mL容量瓶中,加水溶解并稀释至刻度A.AB.BC.CD.D4.(6分)NA为阿伏加德罗常数的值.下列说法正确的是()A.0.1mol的11B中,含有0.6NA个中子B.pH=1的H3PO4溶液中,含有0.1NA个H+C.2.24L(标准状况)苯在O2中完全燃烧,得到0.6NA个CO2分子D.密闭容器中1molPCl3与1molCl2反应制备PCl5(g),增加2NA个PCl﹣键5.(6分)全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a第1页(共28页)常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8)。下列说法错误的是()A.电池工作时,正极可发生反应:2Li2S6+2Li++2e﹣=3Li2S4B.电池工作时,外电路中流过0.02mol电子,负极材料减重0.14gC.石墨烯的作用主要是提高电极a的导电性D.电池充电时间越长,电池中的Li2S2量越多6.(6分)短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外电子数之和为21.下列关系正确的是()WXYZA.氢化物沸点:W<ZB.氧化物对应水化物的酸性:Y>WC.化合物熔点:Y2X3<YZ3D.简单离子的半径:Y<X7.(6分)在湿法炼锌的电解循环溶液中,较高浓度的Cl﹣会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl﹣.根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是()A.Ksp(CuCl)的数量级为107﹣第2页(共28页)B.除Cl﹣反应为Cu+Cu2++2Cl﹣=2CuClC.加入Cu...