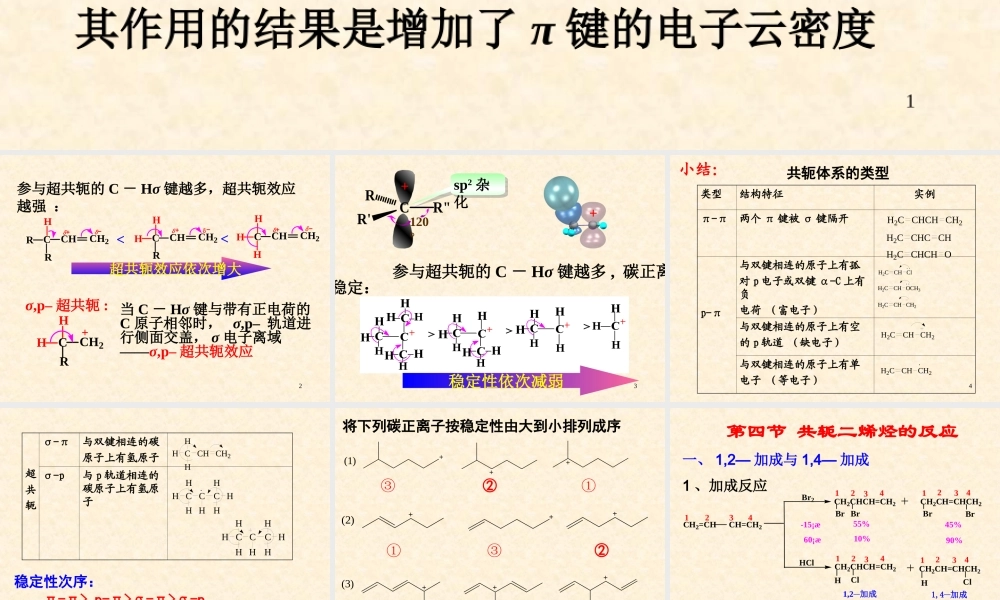
1超共轭(hyperconjugation)σ,π–超共轭:CHHHCHCH2丙烯当C-Hσ键与π键相邻时,两者进行侧面交盖,σ电子离域——σ,π–超共轭效应其作用的结果是增加了π键的电子云密度2参与超共轭的C-Hσ键越多,超共轭效应越强:CRHRCHCH2δδCHHRCHCH2δδCHHHCHCH2δδ<<超共轭效应依次增大σ,p–超共轭:当C-Hσ键与带有正电荷的C原子相邻时,σ,p–轨道进行侧面交盖,σ电子离域——σ,p–超共轭效应CRHHCH23++CRR'R"120°sp2杂化参与超共轭的C-Hσ键越多,碳正离稳定:稳定性依次减弱4共轭体系的类型类型结构特征实例π-π两个π键被σ键隔开p-π与双键相连的原子上有孤对p电子或双键α-C上有负电荷(富电子)与双键相连的原子上有空的p轨道(缺电子)与双键相连的原子上有单电子(等电子)H2CCHCHCH2H2CCHCHOH2CCHCCHH2CCHClH2CCHOCH3H2CCHCH2H2CCHCH2H2CCHCH2小结:5超共轭σ-π与双键相连的碳原子上有氢原子σ-p与p轨道相连的碳原子上有氢原子CHHHCHCH2CHHHCCHHHHCHHHCCHHHH稳定性次序:π-π>p-π>σ-π>σ-p6将下列碳正离子按稳定性由大到小排列成序(1)(2)(3)①②③①②③①②③7一、1,2—加成与1,4—加成1、加成反应55%45%10%90%-15¡æ60¡æCH2=CHCH=CH21234Br2HClCH2CHCH=CH2BrBrBrBrCH2CH=CHCH212341234CH2CH=CHCH2CH2CHCH=CH2HClClH1,2__加成1,4__加成1234123475%20%25%75%<20¡æ>20¡æ第四节共轭二烯烃的反应82、加成反应历程CH2=CHCH=CH2¦Ä¦Ä+¦Ä¦Ä+CH2CH2CH=CH2+1¡£Ì¼ÕýÀë×ÓCH2=CHCHCH3+CH2=CHCHCH3++H+Ï©±û»ù̼ÕýÀë×ÓaabbÎȶ¨ÐÔ:¡Ä¦Ä+CH2CHCHCH3+4321Br¢Ù¢Ú¦Ä+CH2=CHCHCH3Br¢Ù°´°´¢ÚCH2=CHCHCH3Br1,4—加成1,2—加成9CH2=CHCH=CH2+HBr-80C¡£¡£¼Ó³É²úÎï1,2-¼Ó³É²úÎï1,4-81%19%20%80%40C103、热力学控制与动力学控制分析:(1)、1,2—加成活化能低,反应速度快,低温下主要生成1,2—加成产物,1,2—加成产物叫速度(或动力学)控制产物。(2)、1,4—加成活化能高,加成速度慢,高温有利于1,4—加成的进行,1,4—加成产物叫平衡(或热力学)控制产物.(3)、1,2—加成产物对称性差,易分解;1,4—加成产物对称性好,稳定不易分解.结论:缩短反应时间降低反应温度有利于1,2—加成产物的生成;延长反应时间提高反应温度有利于1,4—加成产物的生成。114、溶剂对反应的影响极性溶剂:1,4加成产物为主非极性溶剂:1,2加成产物为主一般情况下,除非特殊说明...