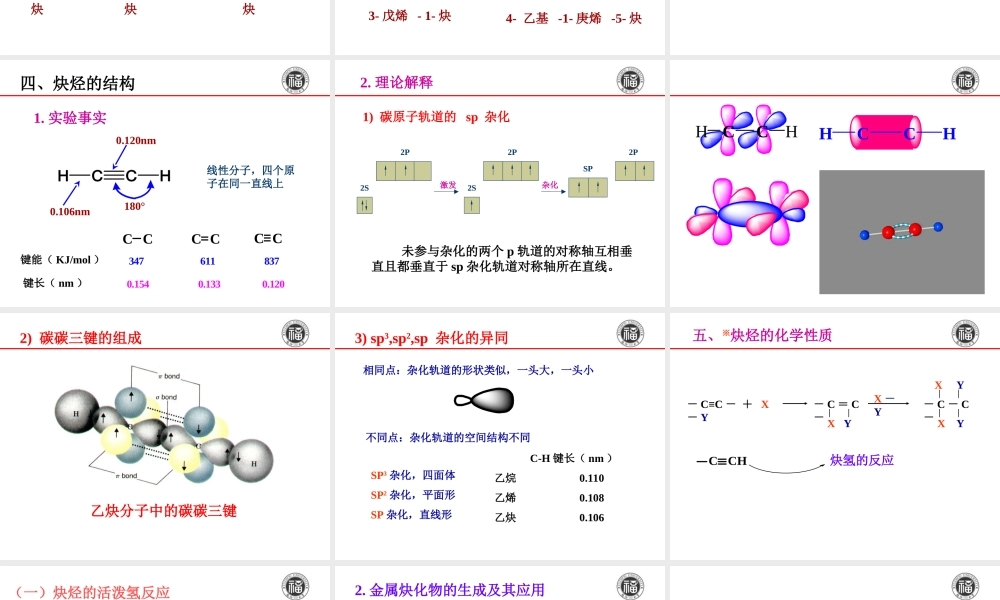
有机化学(OrganicChemistry)第四章炔烃和二烯烃(alkynesanddienes)通式炔烃CnH2n-2官能团二烯烃CnH2n-2CCCCCC一、炔烃的同分异构二、炔烃的命名三、炔烃的物理性质四、炔烃的结构▲五、炔烃的化学性质*六、炔烃的用途炔烃的主要内容一、炔烃的同分异构含有四个或四个以上碳原子的炔烃不仅存在碳链异构还存在官能团位置异构,与烯烃相似。CH3CH2CH2CCHCCHCHCH3CH3CH3CH2CCCH3C≡C-C-CC注意:× 叁键不能有支链,∴无顺反异构体,因此炔烃的异构体数目比烯烃少,比烯烃简单二、炔烃的命名1.与烯烃相似,选择含有C≡C为主链,使其编号最小HCCCCHCH3CH3H3CCH2CH3123453,4-二甲基-3-乙基-1-戊炔CH3CHCH2CCHCH3CH3CHCCCHCH3CH3CH3CH3CHCH2CCCH3CH34-甲基-1-戊炔2,5-二甲基-3-己炔5-甲基-2-己炔2.分子中同时含有C=C和C≡C1)主链选择:含C=C和C≡C在内的最长碳链2)编号:烯加炔的编号和最小;若双键和三键处于相同的位次供选择时,优先给双键最低编号。3)命名:先烯后炔,C数写在烯之前()-某烯-()-炔CCHCHCH3CHCH3CCCHCH2CHC2H5CH23-戊烯-1-炔4-乙基-1-庚烯-5-炔HCCCHCH2CH3CCCHCH2CHCHCHCH3CH21-丁烯-3-炔5-乙烯基-2-辛烯-6-炔三、炔烃的物理性质(P67)四、炔烃的结构1.实验事实CCHH0.120nm0.106nm180°线性分子,四个原子在同一直线上CCCCCC3476118370.1540.1330.120键能(KJ/mol)键长(nm)2.理论解释SP2P1)碳原子轨道的sp杂化2S2P激发2P2S杂化未参与杂化的两个p轨道的对称轴互相垂直且都垂直于sp杂化轨道对称轴所在直线。HCCHHCCH2)碳碳三键的组成乙炔分子中的碳碳三键3)sp3,sp2,sp杂化的异同相同点:杂化轨道的形状类似,一头大,一头小不同点:杂化轨道的空间结构不同SP3杂化,四面体SP2杂化,平面形SP杂化,直线形C-H键长(nm)乙烷0.110乙烯0.108乙炔0.106五、※炔烃的化学性质-C≡C-+X-Y-C=C-XYX-Y-C-C-XXYYCCH炔氢的反应(一)炔烃的活泼氢反应碳原子的杂化状态SPSP2SP3s成分(%)503325电负性3.292.732.481.炔氢的酸性末端炔烃酸性比水、醇弱,但比氨强CH3CH3CH2CH2NH3CHCHEtOHH2OpKa504035251615.72.金属炔化物的生成及其应用HCCHNa,110orNaNH2,ÒºNH3,-33oCoCHCCNaNa,190-220orNaNH2,ÒºNH3,-33oCoCNaCCNaÒºNH3,-33oCCH3CH2CH2BrCH3CH2CH2CCCH2CH2CH3CH3CH2CCCH2CH3CH3CH2CCNaÒºNH3,-33oCCH3CH2Br变为烯,烷或卤代烃,合成上的应用卤代烃不能用叔卤代烃CH3CH2CCHNaNH2,ÒºNH3-33oC3.炔烃的鉴定CH3CH2C...