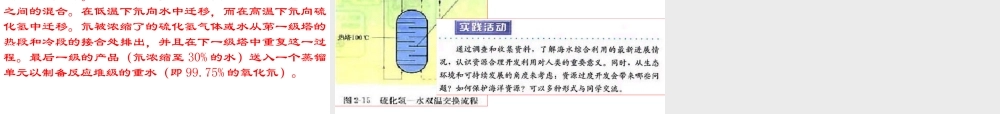
第二课时电解饱和食盐水反应原理阴极:阳极:总反应:2H++2e-=H2↑2Cl--2e-=Cl2↑2H2O+2Cl-=H2↑+Cl2↑+2OH-电解2H2O+2NaCl=H2↑+Cl2↑+2NaOH电解-+Cl2Cl2Cl—H2Na+H+OH—淡盐水NaOH溶液精制饱和NaCl溶液H2O(含少量NaOH)离子交换膜阳极金属钛网阴极碳钢网1、氧化工业上从海水中提取溴时,首先通氯气于pH为3.5左右晒盐后留下苦卤(富含Br-离子)中置换出Br2。二、海水提溴Cl2+2Br-=Br2+2Cl-2.吹出然后用空气把Br2吹出,再用Na2CO3溶液吸收,即得较浓的NaBr和NaBrO3溶液:3CO32-+3Br2=5Br-+BrO33-+3CO2↑最后,用硫酸将溶液酸化,Br2即从溶液中游离出来:5Br-+BrO33-+6H+=3Br2+3H2O3.吸收用还原剂二氧化硫使溴单质变为HBr,再用氯气将其氧化成溴产品。Br2+SO2+2H2O=2HBr+H2SO4Cl2+2Br-=Br2+2Cl-思考:1.海水是一种混合溶液,其中主要含有哪些离子?Cl-Na+Mg2+Ca2+SO42-K+……2.结合海水资源的特点,我们从海水中提取镁到底有没有实际意义?在提取过程中又可能会面临怎样的困难?三、海水提镁思考:1、如何实现Mg2+的富集和分离?可以加入一种试剂使Mg2+沉淀2、是不是直接往海水中加沉淀剂?不是,因为海水中的Mg2+的浓度很小,直接加沉淀剂不利于Mg2+的沉淀,而且会增大沉淀剂的用量,我们可以先将海水浓缩,再加沉淀剂3、从综合角度考虑选用哪种试剂作沉淀剂好?Ca(OH)2思考:如何由贝壳制得氢氧化钙?贝壳(CaCO3)煅烧CaOCa(OH)21、从沉淀效果看,澄清石灰水比氢氧化钠效果差得多,如何解决这一矛盾?3、如何制得无水MgCl2?4、由MgCl2到Mg究竟用还原法还是电解法好?思考:用石灰乳代替石灰水先加盐酸反应,再浓缩得MgCl2·6H2O晶体,然后再将MgCl2·6H2O晶体在HCl气氛中加热脱水即可得无水MgCl2由于镁本身比较活泼,用还原法比较困难,工业上常使用电解熔融的氯化镁得到镁2、请设计由Mg(OH)2到Mg的可能途径。过滤,加盐酸加热电解海水母液bc煅烧a浓缩贝壳石灰乳a;b;c。MgCl2溶液[练习]根据讨论,在下列方框中填入合适的物质的化学式完成工业上用海水提镁的工艺流程,并写出a、b、c三个步骤的化学方程式:CaOMg(OH)2MgCl2·6H2OMgCl2MgMgCl2+Ca(OH)2=Mg(OH)2+CaCl2Mg(OH)Mg(OH)22+2HCl=MgCl+2HCl=MgCl22+2H+2H22OOMgClMgCl22((熔融熔融))==Mg+ClMg+Cl22通电思考:电解产生的Cl2怎么处理?Cl2探究一:取一小段除去氧化膜的镁条投入盛有一定量稀盐酸的试管中;现象:结论或化学方程式:镁条逐渐溶解,有大量气体产生Mg+2HCl=MgCl2+H...