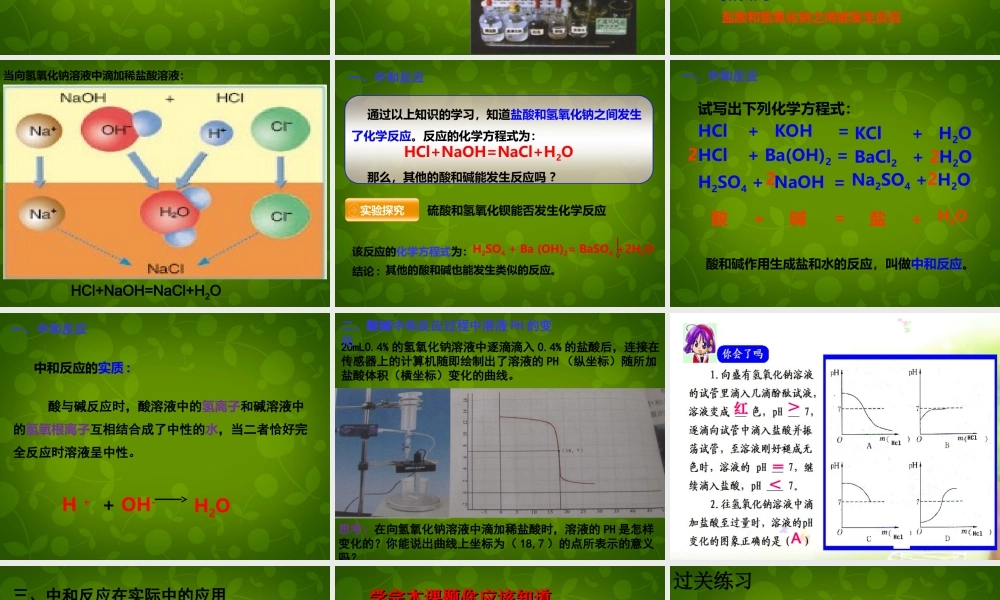
①常见的酸:盐酸(HCl)、硫酸(HSO)₂₄、碳酸(H2CO3)、硝酸(HNO3)读作:某酸②常见的碱:氢氧化钠(NaOH)、氢氧化钾(KOH)氢氧化钙(Ca(OH)2)氨水(NH3•H2O)读作:氢氧化某(1)紫色石蕊试液在酸性溶液中变,在碱性溶液中变。(2)无色酚酞试液在酸性溶液中不变色,在碱性溶液中变。1、溶液的酸碱性可用测定红色酸碱指示剂蓝色红色•2、溶液酸碱性的强弱程度叫酸碱度,用pH值表示:pH=7时溶液显中性7酸性增强014碱性增强pH值越小,酸性越强;pH值越大,碱性越强。小华的妈妈不小心把面团发酸了,你能帮他去掉酸味吗?【思考】第七单元常见的酸和碱第四节酸碱中和反应1、提出问题:盐酸和氢氧化钠之间能否发生反应2、猜想与假设:能发生反应向5%的氢氧化钠中滴加5%的稀盐酸溶液。3、设计实验方案:NaOHHCl4、进行实验探究5、获得结论3、设计实验方案:(1)取少量5%的NaOH溶液(10ml)于烧杯中(2)滴加2-3滴无色酚酞试液,溶液变红(3)向烧杯中滴加稀盐酸,并用玻璃棒不断搅拌,直至溶液由红色变为无色。盐酸和氢氧化钠之间能发生反应当向氢氧化钠溶液中滴加稀盐酸溶液:(1)当滴入稀盐酸溶液量较少时,氢氧化钠有剩余,溶液显___性,溶液显_____色。(2)当滴入稀盐酸溶液量与氢氧化钠恰好完全反应时,溶液显____性,溶液显_____色。(3)当滴入稀盐酸溶液量过量时,稀盐酸有剩余,溶液显_____性,溶液显_____色。碱红中无无酸HCl+NaOH=NaCl+H2O通过以上知识的学习,知道盐酸和氢氧化钠之间发生了化学反应。反应的化学方程式为:HCl+NaOH=NaCl+H2O那么,其他的酸和碱能发生反应吗?一、中和反应实验探究硫酸和氢氧化钡能否发生化学反应该反应的化学方程式为:结论:其他的酸和碱也能发生类似的反应。H2SO4+Ba(OH)2=BaSO4+2H2O试写出下列化学方程式:HCl+KOH=HCl+Ba(OH)2=H2SO4+NaOH=一、中和反应KCl+H2OBaCl2+H2O22Na2SO4+H2O22酸+碱=盐+H2O酸和碱作用生成盐和水的反应,叫做中和反应。中和反应的实质:酸与碱反应时,酸溶液中的氢离子和碱溶液中的氢氧根离子互相结合成了中性的水,当二者恰好完全反应时溶液呈中性。一、中和反应H++OH-H2O20mL0.4%的氢氧化钠溶液中逐滴滴入0.4%的盐酸后,连接在传感器上的计算机随即绘制出了溶液的PH(纵坐标)随所加盐酸体积(横坐标)变化的曲线。思考:在向氢氧化钠溶液中滴加稀盐酸时,溶液的PH是怎样变化的?你能说出曲线上坐标为(18,7)的点所表示的意义吗?二、酸碱中和反应过程中溶液PH的变化红>...