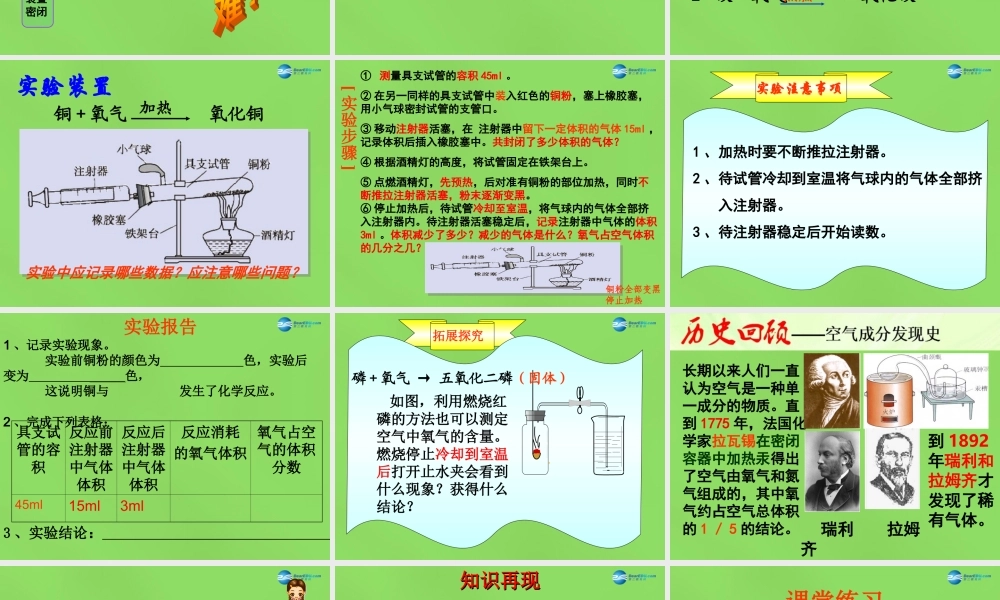
第一节空气的成分氩气0.934%二氧化碳0.003%其他气体0.002%其他成分1%氮气(78%)氧气(21%)洁净干燥空气的成分(体积分数)结论结论空气是一种混合物。空气是一种混合物。思路2:用药品通过化学反应将其他气体除去,只剩下氧气,测定氧气体积。思路1:用药品通过化学反应除去氧气,减少的体积即为氧气的体积。取一定量的空气装置密闭实验原理药品只能与氧气反应且不产生其他气体为测定空气中氧气的含量而运用化学方法除去氧气时,选择的药品只能和什么气体反应?在反应中能否再生成其他气体?为测定空气中氧气的含量而运用化学方法除去氧气时,选择的药品只能和什么气体反应?在反应中能否再生成其他气体?交流与讨论交流与讨论点燃A铜+氧气氧化铜(固体)B石蜡+氧气水+二氧化碳C镁+氧气氧化镁(固体)镁+氮气氮化镁(固体)D磷+氧气五氧化二磷(固体)E碳+氧气二氧化碳加热点燃点燃点燃点燃AD我的课堂我做主实验中应记录哪些数据?应注意哪些问题?铜+氧气氧化铜加热实验装置①测量具支试管的容积45ml。②在另一同样的具支试管中装入红色的铜粉,塞上橡胶塞,用小气球密封试管的支管口。③移动注射器活塞,在注射器中留下一定体积的气体15ml,记录体积后插入橡胶塞中。共封闭了多少体积的气体?④根据酒精灯的高度,将试管固定在铁架台上。⑤点燃酒精灯,先预热,后对准有铜粉的部位加热,同时不断推拉注射器活塞,粉末逐渐变黑。⑥停止加热后,待试管冷却至室温,将气球内的气体全部挤入注射器内。待注射器活塞稳定后,记录注射器中气体的体积3ml。体积减少了多少?减少的气体是什么?氧气占空气体积的几分之几?[实验步骤]铜粉全部变黑停止加热实验注意事项1、加热时要不断推拉注射器。2、待试管冷却到室温将气球内的气体全部挤入注射器。3、待注射器稳定后开始读数。实验报告1、记录实验现象。实验前铜粉的颜色为色,实验后变为色,这说明铜与发生了化学反应。2、完成下列表格:具支试管的容积反应前注射器中气体体积反应后注射器中气体体积反应消耗的氧气体积氧气占空气的体积分数45ml15ml3ml3、实验结论:拓展探究如图,利用燃烧红磷的方法也可以测定空气中氧气的含量。燃烧停止冷却到室温后打开止水夹会看到什么现象?获得什么结论?磷+氧气→五氧化二磷(固体)长期以来人们一直认为空气是一种单一成分的物质。直到1775年,法国化学家拉瓦锡在密闭容器中加热汞得出了空气由氧气和氮气组成的,其中氧气约占空气总体积的1/5的结论。到1892年瑞...