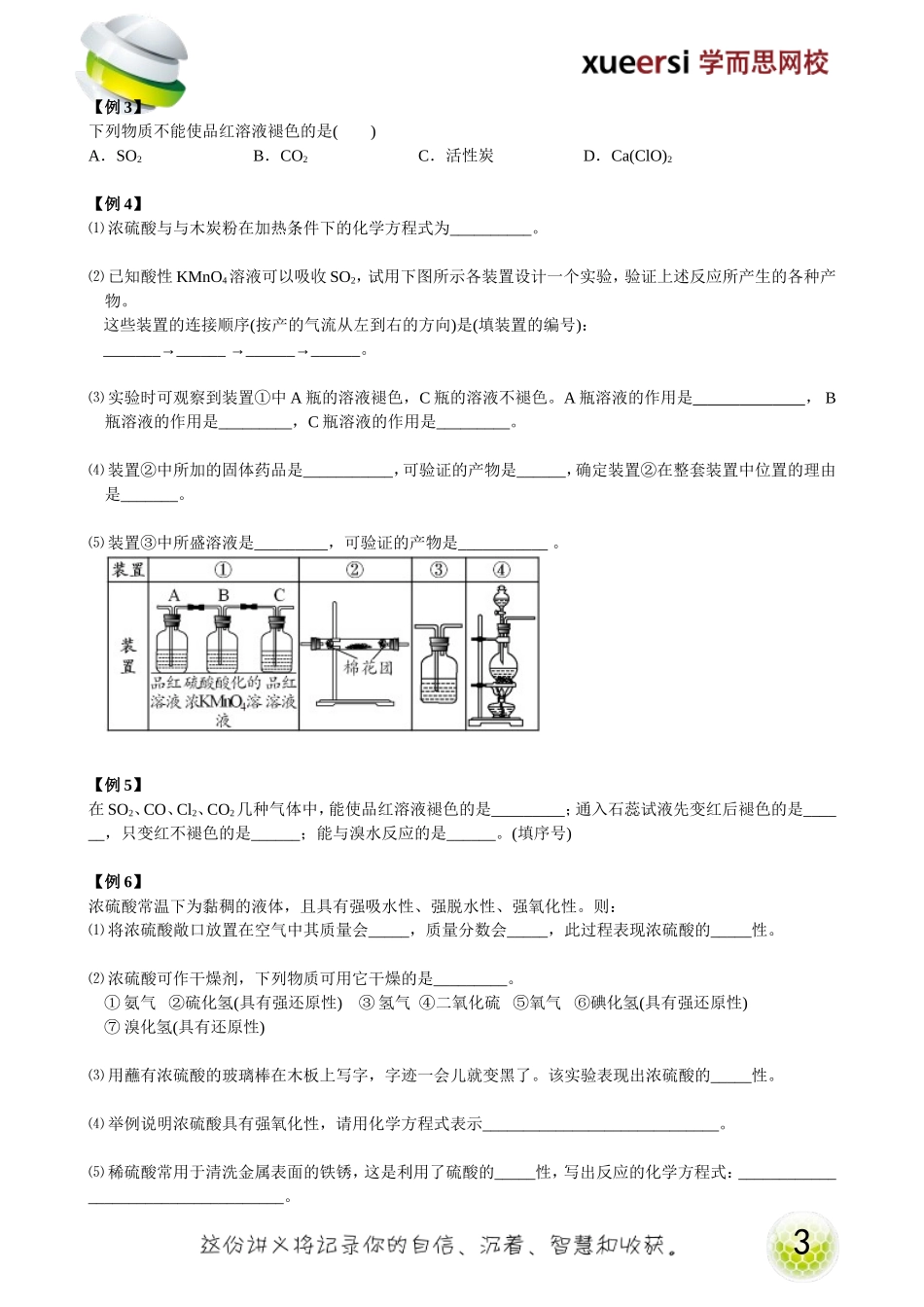
1第一部分:单质硫一、硫原子的结构二、单质硫的性质推测既有氧化性又有还原性以体现氧化性为主三、单质硫的性质1.物理性质硫俗称硫磺,淡黄色固体,质脆,不溶于水,微溶于酒精,易溶于CS2。2.化学性质A.氧化性:①与金属单质反应②与非金属单质反应B.还原性:与氧气反应第二部分:硫的化合物一、硫的氧化物(SO2)1.性质推测既有氧化性又有还原性2.物理性质无色、刺激性气味、有毒、密度比空气大,易液化,易溶于水(1∶40)3.化学性质A.氧化性:B.还原性:SO2+Cl2+2H2O=H2SO4+2HClSO2+Br2+2H2O=H2SO4+2HBr(可使溴水褪色)硫和硫的化合物2SO2具有还原性,还可以使酸性KMnO4溶液褪色C.酸性氧化物a.与H2O反应:SO2+H2OH2SO3b.与碱反应:SO2+2NaOH=Na2SO3+H2OSO2+Ca(OH)2=CaSO3↓+H2O(SO2也可使澄清石灰水变浑浊)c.与碱性氧化物反应:SO2+CaO=CaSO3D.漂白性SO2能与有机色质化合成不稳定的化合物,受热易分解复原。SO2可使品红褪色,加热又恢复为红色,可用于检验SO2。二、硫酸(H2SO4)1.稀硫酸酸的通性2.浓硫酸A.吸水性B.脱水性C.强氧化性a.钝化常温使铁、铝等金属表面形成致密的氧化膜,阻值酸与内部金属反应b.加热时与金属反应c.与非金属单质反应三、硫酸盐盐的通性第三部分:经典练习【例1】下列关于SO2的叙述中,不正确的是()A.常温下可氧化为三氧化硫B.可使品红溶液褪色C.能用浓硫酸干燥D.只有还原性【例2】飘尘是物质燃烧时产生的粒状漂浮物,颗粒很小,不易沉降。它与空气中的二氧化硫和氧气接触时,部分二氧化硫会转化为三氧化硫,使空气中的酸度增加。⑴飘尘所起的作用可能是()A.氧化剂B.还原剂C.催化剂D.载体⑵工业上,二氧化硫被氧化成三氧化硫的化学方程式为________________。3【例3】下列物质不能使品红溶液褪色的是()A.SO2B.CO2C.活性炭D.Ca(ClO)2【例4】⑴浓硫酸与与木炭粉在加热条件下的化学方程式为__________。⑵已知酸性KMnO4溶液可以吸收SO2,试用下图所示各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产的气流从左到右的方向)是(填装置的编号):_______→______→______→______。⑶实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是,B瓶溶液的作用是_________,C瓶溶液的作用是_________。⑷装置②中所加的固体药品是___________,可验证的产物是______,确定装置②在整套装置中位置的理由是_______。⑸装置③中所盛溶液...